พฤติกรรมของแก๊ส
แก๊ส (gas)
แก๊ส เป็นสถานะหนึ่งของสสาร (อันได้แก่ ของแข็ง ของเหลว แก๊ส และพลาสมา) ซึ่งจะกลายเป็นของแข็งได้เมื่ออุณหภูมิลดลง การเปลี่ยนสถานะของสารจากของแข็ง เป็นของเหลวและแก๊ส แสดงดังภาพ

ภาพที่ 1 กลุ่มแก๊ส
ที่มา https://commons.wikimedia.org/wiki/File:Gas_model.png
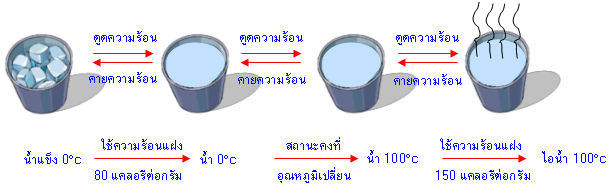
ภาพที่ 2 การเปลี่ยนสถานะของสารจากของแข็ง เป็นของเหลวและแก๊ส
ที่มา http://idchayapks.blogspot.com/2015/07/blog-post.html
ประเภทของแก๊ส
- แก๊สอุดมคติ (Ideal gas) หรือแก๊สสมบูรณ์ เป็นแก๊สที่ นักวิทยาศาสตร์กำหนดขึ้นเพื่ออธิบายสมบัติต่าง ๆ ที่เกี่ยวกับแก๊ส โดยให้มีพฤติกรรมเป็นไปตามทฤษฎีจลน์ของแก๊สไม่ว่าที่อุณหภูมิหรือความดันใด แก๊สสมบูรณ์เป็นแก๊สที่ไม่มีแรงยึดเหนี่ยวระหว่างโมเลกุล
- แก๊สจริง (Real gas) เป็นแก๊สที่มีอยู่จริงในธรรมชาติ และไม่เป็นไปตามกฎต่าง ๆ ของแก๊สสมบูรณ์ มีแรงยึดเหนี่ยวระหว่างโมเลกุลน้อย แต่ในบางสภาวะแก๊สจริงอาจมีสมบัติใกล้เคียงกับแก๊สสมบูรณ์ได้ คือที่อุณหภูมิสูงและความดันต่ำมาก ๆ แก๊สจริงที่มีสมบัติใกล้เคียงกับแก๊สสมบูรณ์ในสภาวะปกติมากที่สุดคือแก๊สเฉื่อยหรือแก๊สในหมู่ที่ 8 ของตารางธาตุ
ก๊าซมีสมบัติโดยทั่ว ๆ ไปดังนี้
1.ก๊าซมีรูปร่างและปริมาตรไม่แน่นอน ขึ้นอยู่กับภาชนะที่บรรจุ ถ้าภาชนะมีรูปร่างและ ปริมาตรอย่างไร ก๊าซจะมีรูปร่างและปริมาตรเป็นอย่างนั้น เช่น เมื่อบรรจุก๊าซจำนวนหนึ่งลงในถังรูปลูกบาศก์ที่มีปริมาตร 10 ลิตร จะได้ก๊าซที่มีปริมาตร 10 ลิตร และมีรูปร่างเป็นรูปลูกบาศก์ตามถังนั้น การที่เป็นเช่นนี้เพราะก๊าซมีการแพร่หรือฟุ้งกระจายได้อย่างอิสระจนเต็มภาชนะเสมอ
2.ก๊าซมีการเคลื่อนที่ตลอดเวลาโดยมีทิศทางการเคลื่อนที่ไม่แน่นอน (Random Motion) กล่าวคือ ก๊าซจะเคลื่อนที่ออกจากจุด ๆ หนึ่งอย่างไม่เป็นระเบียบหรืออย่างอิสระทุกทิศทางซึ่งต่างจากของแข็ง ที่อนุภาคเกือบจะเคลื่อนที่ไม่ได้เลย หรือของเหลวที่อนุภาคเคลื่อนที่ได้บ้าง แต่มีขอบเขตของการเคลื่อนที่ค่อนข้างจำกัด การที่ก๊าซเคลื่อนที่ได้ง่ายกว่าหรือได้เร็วกว่า แสดงว่ามีพลังงานจลน์มากกว่า
3.ก๊าซแพร่ได้เร็วกว่าเพราะแรงยึดเหนี่ยวระหว่างอนุภาคน้อยกว่าของเหลวและของแข็งซึ่งเป็นเหตุให้โมเลกุลของก๊าซแยกจากกันได้ง่าย
4.ที่อุณหภูมิและความดันหนึ่ง ๆก๊าซมีความหนาแน่นน้อยกว่าของเหลวและของแข็ง
5.โดยทั่ว ๆ ไปก๊าซจะมีลักษณะโปร่งใสซึ่งมนุษย์สมารถมองทะลุผ่านไปได้ ก๊าซบางชนิดอาจจะมีสมบัติเฉพาะตัว เช่น มีกลิ่น หรือสีที่แตกต่างจากก๊าซอื่น ๆ เช่น ก๊าซ F2 (สีเหลืองอ่อน) , Cl2 (สีเขียวตองอ่อน) , Br2 (สีแดง) , I2 (สีม่วงแดง) , NO2 (สีน้ำตาลแดง) , SO2 (มีกลิ่นฉุนแสบจมูก) และ H2S (มีกลิ่นก๊าซไข่เน่า) เป็นต้น
6.ปริมาตรของก๊าซขึ้นอยู่กับอุณหภูมิและความดัน ถ้าอุณหภูมิและความดันเปลี่ยนไปจะทำให่ปริมาตรเปลี่ยนไปด้วย เนื่องจากสมบัติของก๊าซขึ้นอยู่กับอุณหภูมิและความดัน ดังนั้นในการกล่าวถึงปริมาตรของก๊าซ จึงต้องระบุอุณหภูมิและความดันควบคู่กันไปทุกครั้ง ถ้าไม่ระบุอาจจะถือว่าให้ความหมายไม่สมบูรณ์ เช่น ก๊าซ H2 มีปริมาตร 22.4 ลิตร ที่ 0 0C , 1 atm จัดว่ามีข้อมูลที่สมบูรณ์
อุณหภูมิ ใช้สัญลักษณ์เป็น T (เคลวิน) และ t (เซลเซียส) เป็นมาตราส่วนที่ใช้บอกระดับความร้อนของสาร แต่ไม่ได้บอกให้ทราบว่าสารนั้นมีปริมาณความร้อนเท่าใด การกำหนดมาตราส่วนของอุณหภูมิในเทอร์โมมิเตอร์มักจะใช้จุดเยือกแข็งและจุดเดือดของของเหลว เช่น น้ำเป็นหลัก โดยการวัดจุดเยือกแข็งและจุดเดือดของน้ำที่ความดัน 1 บรรยากาศ แล้วแบ่งช่วงระยะระหว่างจุดเดือดกับจุดเยือกแข็งออกเป็นช่องเท่า ๆ กันตามความต้องการ กลายเป็นมาตราส่วนอุณหภูมิ เช่น แบ่งออกเป็น 100 ช่อง ๆ เท่า ๆกัน แต่ละช่องเรียกว่า 1 องศา เป็นต้น
ความดัน ใช้สัญลักษณ์เป็น P หมายถึงแรงที่กระทำต่อหนึ่งหน่วยพื้นที่ ความดันเป็นสมบัติอย่างหนึ่งของของไหล (เรียกของเหลวและไอหรือก๊าซรวมกันว่า ของไหล) ความดันสามารถใช้บอกทิศทางการเคลื่อนที่ของอของเหลวและก๊าซได้ คือ ทั้งของเหลวและก๊าซจะเคลื่อนที่จากส่วนที่มีความดันสูงไปสู่ส่วนที่มีความดันต่ำกว่าเสมอ
เครื่องมือที่ใช้วัดความดันเรียกว่า บารอมิเตอร์ (Barometer) ซึ่งมีลักษณะต่าง ๆ กัน บารอมิเตอร์มักจะทำด้วยปรอทซึ่งเป็นของเหลวที่มีความหนาแน่นมาก โดยใช้หลอดแก้วยาวและตรงมีพื้นที่หน้าตัดเท่ากันตลอดขนาด 1 cm2 ยาวประมาณ 100 cm ปลายด้านหนึ่งปิด บรรจุปรอทจนเต็มหลอดแล้วคว่ำปลายด้านเปิดลงบนอ่างปรอท ระดับปรอทจะลดลงเล็กน้อยและทำให้มีที่ว่างตอนบนของหลอดแก้วเป็นสุญญากาศ (ดูในรูป) การที่ปรอทส่วนหนึ่งยังค้างอยู่ภายในหลอดแก้วก็เนื่องจากแรงกดดันของบรรยากาศที่มีต่อผิวหน้าของปรอทในอ่างปรอท ซึ่งแสดงว่ามวลของบรรยากาศหรือความกดดันของบรรยากาศที่มีต่อผิวปรอทในอ่างจะต้องเท่ากับความกดดันที่เกิดจากมวลของปรอทในหลอดแก้ว ซึ่งกดลงมายังอ่างปรอท จึงทำให้ระดับความสูงของปรอท มีค่าคงที่ ดังนั้นความสูงขอลปรอทในหลอดแก้วจึงเท่ากับความดันของบรรยากาศนั่นเอง ถ้าใช้พื้นที่หน้าตัดของหลอดแก้วเท่ากับ 1 cm3 ปกติจะได้ลำปรอทสูงประมาณ 76 cm หรือ 760 mm ซึ่งเรียกว่า 1 บรรยากาศ (atm)
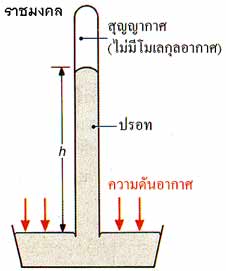
ภาพที่ 3 เครื่องมือวัดความดัน (บารอมิเตอร์)
ที่มา:http://www.neutron.rmutphysics.com/physics/index.php?option=com_content&view=article&id=88:2009-02-16-07-06-53&catid=1:2008-04-22-04-52-20&Itemid=61
อุณหภูมิและความดันมาตรฐาน
ใช้สัญลักษณ์ เป็น STP ซึ่งย่อมาจาก Standard Temperature and Pressure หรือ NTP ซึ่งย่อมาจาก Normal Temperature and Pressure เนื่องจากปริมาตรของก๊าซเปลี่ยนแปลงไปตามอุณหภูมิและความดัน การระบุปริมาตรจึงต้องระบุอุณหภูมิและความดันควบคูกันเสมอ เพื่อความสะดวกสำหรับการเปรียบเทียบปริมาตรของก๊าซจึงได้กำหนดสภาวะอ้างอิงซึ่งเป็นสภาวะมาตรฐานของก๊าซขึ้นมาดังนี้
อุณหภูมิมาตรฐานของก๊าซ คือ 00C หรือ 273.15 K (273 K โดยประมาณ)
ความดันมาตรฐานของก๊าซ คือ 1 atm หรือ 760 mm Hg
ปริมาตรของก๊าซ
ใช้สัญลักษณ์เป็น V หมายถึง ปริมาตรของภาชนะที่บรรจุก๊าซ ทั้งนี้ เพราะถือว่าก๊าซไม่มีปริมาตรโมเลกุล และก๊าซสามารถแพร่กระจายจนเต็มภาชนะที่บรรจุเสมอ ในกรณีของเหลว และของแข็ง การหาปริมาณอาจจะใช้วิธีชั่งมวล เพราะทั้งของแข็งและของเหลวมีมวลมาก หรืออาจจะใช้วัดปริมาตรก็ได้ แต่ในกรณีของก๊าซ ซึ่งมีความหนาแน่นน้อยกว่าของเหลวและของแข็งมาก มวลจึงมีค่าน้อย
หน่วยของปริมาตรที่ใช้กันทั่วไปคือ dm3 และ cm3 ซึ่งเป็นหน่วย S.I และลิตร กับ มิลลิลิตร ซึ่งเป็นหน่วยเมตริก โดยกำหนดให้
1 ลิตร = 1000.027 cm3 = 1 dm3 (โดยประมาณ)
1 มิลลิลิตร = 1.000027 cm3 = 1 cm3 (โดยประมาณ)
เพราะฉะนั้น 1 dm3 = 103 cm3 = 1 ลิตร = 103 มิลลิลิตร
แหล่งที่มา
แฟรงค์ เดวิด วี. (2547). ชุดสำรวจโลกวิทยาศาสตร์องค์ประกอบพื้นฐานทางเคมี. กรุงเทพฯ:
เพียร์สัน เอ็ดดูเคชัน อินโดไชน่า.
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี (สสวท.). (2551).หนังสือเรียนวิทยาศาสตร์พื้นฐาน ชั้นมัธยมศึกษาปีที่ 2 เล่ม 1 กลุ่มสาระการเรียนรู้วิทยาศาสตร์ ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พ.ศ. 2551. กรุงเทพฯ : คุรุสภาลาดพร้าว.
ศรีลักษณ์ พลวัฒนะ, และคณะ.(2551). หนังสือเรียนเสริมฯ สารและสมบัติของสาร ม.4-6 ช.4 สำนักพิมพ์ แม็ค บจก. สนพ.
-
9426 พฤติกรรมของแก๊ส /lesson-chemistry/item/9426-2018-11-14-08-41-26เพิ่มในรายการโปรด


