ทำนายแนวโน้มของธาตุตัวต่อไปในตารางธาตุได้อย่างไร?
ท่านผู้อ่านที่เคยได้เรียนวิชาวิทยาศาสตร์ โดยเฉพาะอย่างยิ่งวิทยาศาสตร์เคมีในชั้นมัธยมศึกษานั้น หนึ่งอย่างที่เคยผ่านกันมานั่นก็คือ การท่องจำตารางธาตุ บางแห่งก็ให้ท่อง 20 ธาตุแรก บางแห่งก็ให้ท่องธาตุทั้ง 8 หมู่ แต่หากคนใดที่ความจำดีอย่างยิ่งยวดแล้วนั้น ก็คงท่องจำธาตุทั้งหมดทุกตัวในตารางธาตุกันเลยทีเดียว ซึ่งในปัจจุบันธาตุในตารางธาตุมีกี่ตัว และจะสิ้นสุดที่ธาตุตัวที่เท่าไหร่นั้น เรามาศึกษาข้อมูลของตารางธาตุกันคร่าว ๆ กันดีกว่า
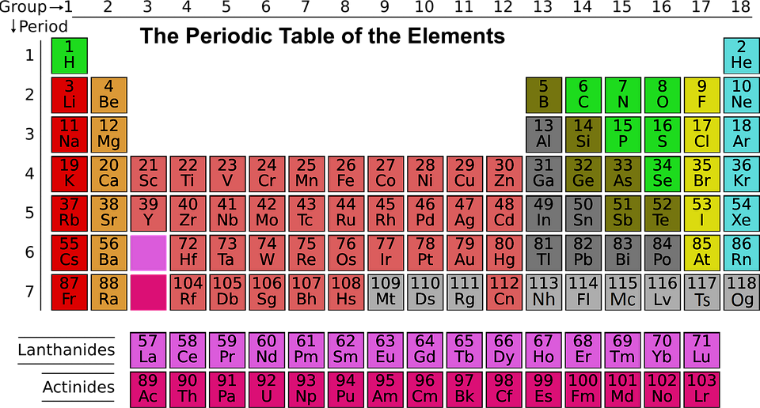
ภาพที่ 1 ตารางธาตุในปัจจุบัน
ที่มา https://pixabay.com/ ,explorersinternational
ตารางธาตุเกิดขึ้นได้อย่างไร?
ในศตวรรษที่ 18 ธาตุถูกค้นพบเพียงไม่กี่ธาตุ โดยนักวิทยาศาสตร์คนแรกคือ โยฮันน์ โวลฟ์กัง เดอเบอไรเนอร์ ซึ่งได้เสนอการจัดแบ่งธาตุออกเป็นกลุ่ม ๆ กลุ่มละ 3 ธาตุ ที่มีคุณสมบัติเหมือน ๆ กัน โดยเรียกการจัดแบบนี้ว่า ไตรแอดส์ (ชุดสาม) โดยพบว่าธาตุตรงกลางจะมีมวลอะตอมเป็นค่าเฉลี่ยของมวลอะตอมอีกสองธาตุที่เหลือ เช่น กลุ่มที่ 1 ได้แก่ธาตุลิเทียม (Li) โซเดียม (Na) โพแทสเซียม (K) ตามหลักการนี้ธาตุโซเดียมซึ่งเป็นธาตุตรงกลางระหว่างธาตุลิเทียมและโพแทสเซียมจะมีมวลอะตอมเป็น 23 ซึ่งเป็นค่าเฉลี่ยของมวลอะตอมของลิเทียมคือ 7 และ โพแทสเซียมคือ 39 แต่ในเวลาต่อมาเมื่อนำหลักการดังกล่าวไปใช้กับธาตุกลุ่มอื่นที่มีสมบัติคล้ายกัน มวลอะตอมของธาตุตรงกลางกลับไม่ได้ตรงกับมวลอะตอมเฉลี่ยของธาตุทั้งสองที่เหลือ หลักการจัดตารางธาตุแบบไตรแอดส์ของเดอเบอไรเนอร์จึงไม่เป็นที่ยอมรับอีกต่อไป
ต่อมาในปี ค.ศ. 1865 จอห์น นิวแลนด์ นักวิทยาศาสตร์ชาวอังกฤษได้เสนอการจัดเรียงธาตุเป็นหมวดหมู่ขึ้นใหม่ โดยเรียงตามลำดับมวลอะตอม นิวแลนด์กล่าวว่าถ้านำธาตุมาเรียงตามลำดับมวลอะตอมแล้ว พบว่า "ธาตุที่ 8 จะมีสมบัติคล้ายคลึงกับธาตุตัวที่ 1 โดยยกเว้นธาตุไฮโดรเจนและแก๊สเฉื่อย" กฎของนิวแลนด์นี้เรียกว่า “Law of octaves” ตัวอย่างเช่น ถ้าเริ่มต้นจากลิเทียม (มวลอะตอม = 7) เป็นธาตุตัวที่ 1 ธาตุโซเดียม (น้ำหนักอะตอม = 23) จะเป็นธาตุตัวที่ 8 โดยธาตุทั้งสองมีสมบัติทางเคมีและทางฟิสิกส์คล้ายคลึงกัน อย่างไรก็ตามการจัดตารางธาตุแบบนิวแลนด์ยังมีข้อจำกัดคือสามารถใช้ได้เพียงแค่น้ำหนักอะตอมไม่เกินธาตุแคลเซียม (Ca) ต่อมาเมื่อมีการค้นพบแก๊สเฉื่อยก็ไม่สามารถจัดตามตารางธาตุของนิวแลนด์ได้และไม่สามารถอธิบายได้ว่าเพราะเหตุใดมวลอะตอมจึงมีความสัมพันธ์กับความคล้ายคลึงกันของสมบัติของธาตุ ตามหลักการดังกล่าว
ต่อมายูลิอุสโลทาร์ ไมเออร์ นักวิทยาศาสตร์ชาวเยอรมัน และดิมิทรี อิวาโนวิช เมนเดเลเอฟ นักวิทยาศาสตร์ชาวรัสเซีย ได้ศึกษารายละเอียดของธาตุต่าง ๆ มากขึ้น และมีข้อสังเกตเป็นอย่างเดียวกันในเวลาใกล้เคียงกันว่า ถ้าจัดเรียงธาตุตามมวลอะตอมจากน้อยไปหามาก ธาตุจะมีสมบัติคล้ายกันเป็นช่วง ๆ ซึ่งเมนเดเลเอฟตั้งเป็นกฎเรียกว่า "กฎพิริออดิก" และได้เสนอความคิดนี้ในปี ค.ศ. 1869 ก่อนที่ไมเออร์จะนำผลงานของเขาออกเผยแพร่ในปีต่อมา และเพื่อเป็นการให้เกียรติแก่เมนเดเลเอฟ จึงใช้ชื่อว่า ตารางพิริออดิกของเมนเดเลเอฟ โดยในตอนนั้นเมนเดเลเอฟได้จัดธาตุที่มีสมบัติคล้ายคลึงกันที่ปรากฏซ้ำกันเป็นช่วง ๆ ให้อยู่ในแนวตั้งหรือหมู่เดียวกันและพยายามเรียงลำดับมวลอะตอมของธาตุจากน้อยไปหามาก ถ้าเรียงตามมวลอะตอมแล้วมีสมบัติไม่สอดคล้องกัน ก็พยายามจัดให้เข้าหมู่โดยเว้นช่องว่างไว้ในตำแหน่งที่คิดว่าน่าจะเป็นธาตุที่ยังไม่มีการค้นพบ และยังได้ใช้สมบัติของธาตุและสารประกอบอื่น ๆ นอกเหนือจากคลอไรด์และออกไซด์มาประกอบการพิจารณาด้วย โดยตำแหน่งของธาตุในตารางจะมีความสัมพันธ์กับสมบัติของธาตุ ซึ่งช่วยให้เมนเดเลเอฟสามารถทำนายสมบัติของธาตุในช่องว่างที่ยังไม่มีการค้นพบได้อย่างใกล้เคียง
เมนเดเลเอฟได้จัดธาตุที่มีสมบัติคล้ายคลึงกันที่ปรากฏซ้ำกันเป็นช่วง ๆ ให้อยู่ในแนวตั้งหรือหมู่เดียวกันและพยายามเรียงลำดับมวลอะตอมของธาตุจากน้อยไปหามาก ถ้าเรียงตามมวลอะตอมแล้วมีสมบัติไม่สอดคล้องกัน ก็พยายามจัดให้เข้าหมู่โดยเว้นช่องว่างไว้ในตำแหน่งที่คิดว่าน่าจะเป็นธาตุที่ยังไม่มีการค้นพบ และยังได้ใช้สมบัติของธาตุและสารประกอบอื่น ๆ นอกเหนือจากคลอไรด์และออกไซด์มาประกอบการพิจารณาด้วย โดยตำแหน่งของธาตุในตารางจะมีความสัมพันธ์กับสมบัติของธาตุ ซึ่งช่วยให้เมนเดเลเอฟสามารถทำนายสมบัติของธาตุในช่องว่างได้อย่างใกล้เคียง

ภาพที่ 2 นักเคมีชาวรัสเซีย ดมีตรี เมนเดเลเยฟ (Dmitriy Ivanovich Mendeleyev)
ที่มา https://en.wikipedia.org/wiki/Dmitri_Mendeleev#/media/File:DIMendeleevCab.jpg
อย่างไรก็ตาม เมนเดเลเอฟไม่สามารถอธิบายได้ว่าเพราะเหตุใดจึงต้องยกเว้นไม่จัดเรียงธาตุตามมวลอะตอมในกรณีที่ธาตุมีสมบัติไม่สอดคล้องกัน เนื่องจากสมัยนั้นนักวิทยาศาสตร์ยังศึกษาโครงสร้างของอะตอมและไอโซโทปได้ไม่ชัดเจน ทำให้นักวิทยาศาสตร์รุ่นต่อมาเกิดแนวความคิดว่า ตำแหน่งของธาตุในตารางธาตุไม่น่าจะขึ้นอยู่กับมวลอะตอมของธาตุ แต่น่าจะขึ้นอยู่กับสมบัติอื่นที่มีความสัมพันธ์กับมวลอะตอม
ปัจจุบันธาตุในตารางธาตุมีกี่ตัวนะ?
สหภาพเคมีบริสุทธิ์และเคมีประยุกต์ระหว่างประเทศ (International Union of Pure and Applied Chemistry หรือ IUPAC) มีมติอย่างเป็นทางการ ประกาศชื่อธาตุใหม่ 4 ตัวในตารางธาตุ ดังต่อไปนี้
-
ธาตุลำดับที่ 113 ชื่อ Nihonium สัญลักษณ์ Nh ค้นพบโดยนักวิทยาศาสตร์จากห้องปฏิบัติการ RIKEN Nishina Center for Accelerator-Based Science (Japan) ประเทศญี่ปุ่น โดย Nh มาจากคำว่า Nihon ซึ่งเป็นคำเรียกชื่อประเทศญี่ปุ่น นับเป็นธาตุแรกที่ถูกค้นพบในเอเชีย
-
ธาตุลำดับที่ 115 ชื่อ Moscovium สัญลักษณ์ Mc ค้นพบโดยนักวิทยาศาสตร์จากห้องปฏิบัติการ Joint Institute for Nuclear Research, Dubna (Russia) ในประเทศรัสเซีย โดยชื่อธาตุได้มาจากชื่อเมือง Moscow ซึ่งเป็นที่ตั้งของสถาบันวิจัยแห่งนี้
-
ธาตุลำดับที่ 117 ชื่อ Tennessine สัญลักษณ์ Ts ค้นพบโดยนักวิทยาศาสตร์จากห้องปฏิบัติการ Oak Ridge National Laboratory (USA), Vanderbilt University (USA), Lawrence Livermore National Laboratory (USA) ซึ่งเป็นผู้ร่วมค้นพบธาตุนี้ ชื่อธาตุตั้งชื่อตามรัฐ Tennessee ประเทศสหรัฐอเมริกา ซึ่งเป็นที่ตั้งของห้องปฏิบัติการแห่งนี้
-
ธาตุลำดับที่ 118 ชื่อ Oganesson สัญลักษณ์ Og ค้นพบโดยทีมวิจัยจากห้องปฏิบัติการ Joint Institute for Nuclear Research, Dubna (Russia) และ Lawrence Livermore National Laboratory (USA) ตั้งชื่อเพื่อเป็นเกียรติแก่ ศาสตราจารย์ Yuri Oganessian ซึ่งยังมีชีวิตและอุทิศตนให้แก่การศึกษาวิจัยธาตุในกลุ่ม superheavy element

ภาพที่ 3 ธาตุตัวที่ 118
ที่มา https://pixabay.com/ ,LJNovaScotia
ธาตุทั้ง 4 เป็นธาตุหนัก (superheavy element) ที่ไม่สามารถพบในธรรมชาติ แต่เป็นธาตุที่สังเคราะห์ขึ้นจากปฏิกิริยานิวเคลียร์ในห้องปฏิบัติการ และเป็นธาตุกัมมันตรังสี แต่ละชนิดมีสมบัติเฉพาะที่แตกต่างกันทั้งการจัดเรียงอิเล็กตรอน มวลอะตอม และจำนวนไอโซโทป การประกาศชื่อธาตุ 4 ธาตุใหม่นี้ ทำให้ตารางธาตุจะมีธาตุครบตั้งแต่เลขอะตอม 1 ไปจนถึงเลขอะตอม 118 ซึ่งทำให้ตารางธาตุคาบที่ 7 เต็มพอดี ถึงแม้ธาตุหนักยิ่งยวดที่สังเคราะห์ขึ้นนี้ไม่เสถียร และจะสลายตัวภายในเวลาเพียงเสี้ยววินาที แต่การสังเคราะห์ธาตุชนิดใหม่ๆนั้น อาจจะทำให้ตารางธาตุขยายไปถึงคาบที่ 8 ได้
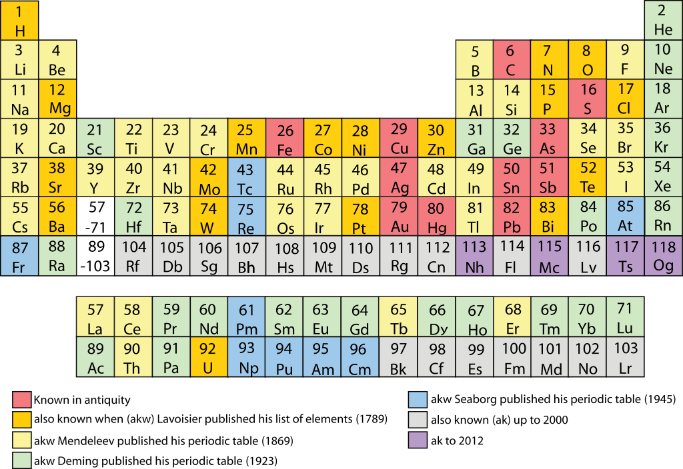
ภาพที่ 4 วิวัฒนาการการค้นพบของธาตุในตารางธาตุตามช่วงระยะเวลา
ที่มา https://th.wikipedia.org
แต่เดิมนักวิทยาศาสตร์คาดว่าธาตุโลหะซูเปอร์เฮฟวี่ (Super-heavy Metal คือธาตุที่มีจำนวนโปรตอน 104 ขึ้นไป) นั้นน่าจะมีค่าครึ่งชีวิตที่ยาวนาน จึงเป็นที่น่าสนใจและพยายามค้นหาธาตุเหล่านั้น แต่ปรากฏว่ายิ่งมีการเพิ่มนิวตรอนและโปรตอนลงไปในนิวเคลียสลงไปมากเท่าใด อะตอมก็ยิ่งมีความเสถียรน้อยลง ธาตุโลหะซูเปอร์เฮฟวี่ส่วนใหญ่จึงอยู่ได้เพียงแค่เพียงไมโครหรือนาโนวินาทีเท่านั้น อย่างไรก็ตามหลังจากมีการสร้างธาตุโลหะซูเปอร์เฮฟวี่ได้มากขึ้นก็มีข้อสังเกตจนกระทั่งตั้งเป็นทฤษฎีที่เกี่ยวกับความเสถียรของธาตุซุปเปอร์เฮฟวี่เหล่านี้ว่า ถ้าเพิ่มจำนวนเลขอะตอมไปถึงค่าๆ หนึ่ง ธาตุซูเปอร์เฮฟวี่ที่ได้ จะมีเสถียรภาพมากและอยู่ได้นานขึ้น เรียกทฤษฎีนี้ว่า Island of stability โดยคาดการณ์กันว่าธาตุตัวที่จะมีเสถียรภาพมากพอที่จะตรวจสอบได้คือธาตุที่ 120 เพราะจะมีสมบัติแบบธาตุหมู่ 2 (แอลคาไลน์ เอิร์ท) ซึ่งปัจจุบันนักวิทยาศาสตร์ก็ยังคงรอคอยการพิสูจน์ทฤษฎีนี้อย่างใจจดใจจ่อ และเราคงต้องรอลุ้นกันต่อไปว่าในอนาคตจะมีธาตุใหม่เกิดขึ้นอีกจำนวนมากน้อยเพียงใด และจะสิ้นสุดที่ธาตุตัวใด
แหล่งที่มา
ปุณิกา พระพุทธคุณ (2561) 4 ธาตุใหม่เติมเต็มตารางธาตุในคาบ 7. รอบรู้วิทย์, 46(210) มกราคม – กุมภาพันธ์ 2561, 7 – 9.
อัจฉราพรรณ โพธิ์ทอง . ธาตุใหม่ เติมเต็มตารางธาตุ . สืบค้นเมื่อ 4 เมษายน 2562. จาก https://il.mahidol.ac.th/th/i-Learning-Clinic/chemistry-articles/ธาตุใหม่-เติมเต็มตารางธ/
IUPAC ANNOUNCES THE NAMES OF THE ELEMENTS 113, 115, 117, AND 118. Retrieved April 4, 2019, from https://iupac.org/iupac-announces-the-names-of-the-elements-113-115-117-and-118/



