เคมีของอินดิเคเตอร์
อินดิเคเตอร์ (Indicator) คือ สารที่ใช้บอกความเป็นกรด-เบส ของสารละลายได้อย่างหนึ่ง สารประกอบที่เปลี่ยนสีได้ที่ pH เฉพาะตัว จะถูกนำมาใช้เป็นอินดิเคเตอร์ได้ เช่น ฟีนอล์ฟทาลีน จะไม่มีสีเมื่ออยู่ในสารละลายกรด และจะเปลี่ยนเป็นสีชมพู เมื่ออยู่ในสารละลายเบสที่มี pH 8.3 ซึ่งสีของอินดิเคเตอร์
แต่ละชนิด จะเปลี่ยนในช่วง pH ที่ต่างกัน ซึ่งแสดงได้ดังภาพ
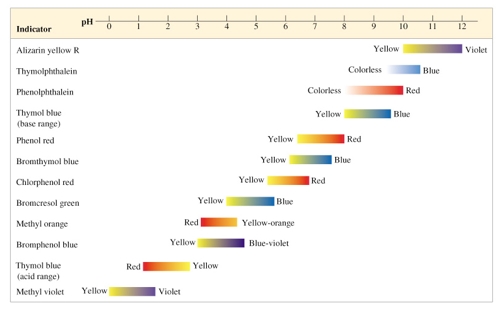
ภาพที่ 1 ค่า pH ของอินดิเคเตอร์แต่ละชนิด
ที่มา https://il.mahidol.ac.th/e-media/acid-base/C8.HTM

ภาพที่ 2 ค่า ph ค่า pH บอกค่าความเป็นกรด-กลาง-ด่าง
ที่มา https://www.freepik.com/premium-vector/ph-value-scale-meter-acid-alkaline-solutions_6332240.htm#position=4
การหา pH ของสารละลายโดยใช้อินดิเคเตอร์หลาย ๆ ชนิดนี้ ไม่สะดวกในการใช้จึงมีการคิดที่จะนำอินดิเคเตอร์หลาย ๆ ชนิด ซึ่งเปลี่ยนสีในช่วง pH ต่าง ๆ กันมาผสมกันในสัดส่วนที่เหมาะสม จะสามารถใช้บอกค่า pH ของสารละลายได้ละเอียดขึ้น อินดิเคเตอร์ผสมนี้เรียกว่า ยูนิเวอร์ซัลอินดิเคเตอร์ ซึ่งสามารถเปลี่ยนสีได้ในสารละลายที่มี pH ต่าง ๆ กันเกือบทุกค่า
การใช้ยูนิเวอร์ซัลอินดิเคเตอร์ หยดยูนิเวอร์ซัลอินดิเคเตอร์ลงในสารละลายที่ต้องการหาค่า pH ประมาณ 3 หยดต่อสารละลาย 3 cm3 สังเกตสีของสารละลายแล้วเปรียบเทียบกับสีมาตรฐานของยูนิเวอร์ซัลอินดิเคเตอร์ที่ pH ต่าง ๆ ว่าสีของสารละลายตรงกับสีมาตรฐานที่ pH ใด ก็จะมีค่าเท่ากับ pH นั้น
อินดิเคเตอร์มีประโยชน์อย่างไรในปฏิกิริยาเคมี?
ตามที่ได้กล่าวถึงก่อนนี้ว่า อินดิเคเตอร์ คือสารที่ใช้บอกความเป็นกรด-เบส ของสารละลาย ซึ่งปฏิกิริยาในการสังเกตว่ากรดหรือเบสทำปฏิกิริยากัน ณ จุดใดนั้น เราต้องทำการไทเทรตเพื่อหาจุดยุติหรือจุดสมมูลของการเกิดปฏิกิริยาดังกล่าว ซึ่งการไทเทรต คือ วิธีการทางปริมาณวิเคราะห์ (Quantitative Analysis) ใช้ในการหาปริมาตรของสารละลายมาตรฐาน (สารละลายที่เราทราบความเข้มข้นที่แน่นอนแล้ว) ที่ทำปฏิกิริยาพอดีกับสารละลายอื่นซึ่งทราบปริมาตร แต่ยังไม่ทราบความเข้มข้น เพื่อนำค่าปริมาตรที่ได้มาคำนวณหาความเข้มข้นของสารละลายอื่นนั้น
สำหรับการไทเทรตทุกชนิด จุดที่สารที่เรานำมาไทเทรตทำปฏิกิริยากันพอดี เราเรียกว่า จุดสมมูลหรือจุดสะเทิน (Equivalence Point) จุดที่กรดทำปฏิกิริยากันพอดีหรือสะเทินพอดีกับเบส ส่วนจุดที่อินดิเคเตอร์ (Indicator) เปลี่ยนสี เราเรียกว่า จุดยุติ (End Point) ซึ่งเป็นจุดที่เราจะยุติการไทเทรต โดยถ้าเราใช้อินดิเคเตอร์ที่เหมาะสมจะทำให้จุดยุติตรงกับจุดสมมูลหรือใกล้เคียงกับจุดสมมูลมาก แต่ถ้าเราใช้อินดิเคเตอร์ไม่เหมาะสมอาจจะทำให้จุดยุติอยู่ห่างจากจุดสมมูลมาก ทำให้ผลการทดลองคลาดเคลื่อนได้
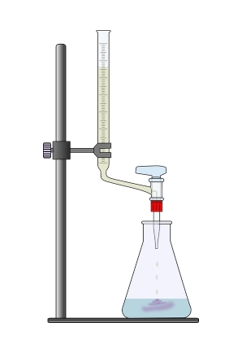
ภาพที่ 2 การไทเทรตกรด-เบส
ที่มา https://www.pixabay.com, OpenClipAart-Vectors
อินดิเคเตอร์ในธรรมชาติ (Natural indicator)
จากที่กล่าวมาข้างต้นจะเห็นได้ว่าอินดิเคเตอร์ที่ถูกใช้ในการไทเทรตนั้นส่วนใหญ่มาจากการสังเคราะห์ขึ้น ซึ่งในประเทศที่มีความเจริญก้าวหน้าทางด้านวิทยาศาสตร์และเทคโนโลยี รวมถึงการหันมาใช้อินดิเคเตอร์จากธรรมชาติเพิ่มมากขึ้น นอกจากจะช่วยลดการใช้สารเคมีแล้วนั้น ยังมีงานวิจัยถึงคุณสมบัติของสารในธรรมชาติเพื่อนำมาใช้เป็นอินดิเคเตอร์อีกหลายๆ หน่วยงานและองค์กรได้ทำการศึกษาอินดิเคเตอร์จากธรรมชาติมากมาย เช่นเดียวกับงานวิจัยของมหาวิทยาลัยบูรพาที่นำเอาพืชในท้องถิ่น เช่น แก่นฝาง และหมามุ่ยมาสกัดและทำเป็นอินดิเคเตอร์ ซึ่งพบว่าพืชทั้งสองชนิดสามารถนำมาใช้เป็นอินดิเคเตอร์ในปฏิกิริยาเคมีได้ไม่แตกต่างกับสารเคมีอื่นๆ ที่ใช้ในห้องปฏิบัติการเลย หรือหลายๆ งานวิจัยนำเอาสารสกัดจากเปลือกแก้วมังกรมาใช้เป็นอินดิเคเตอร์ นอกจากนี้ยังมีอินดิเคเตอร์จากธรรมชาติอีกหลายๆ ชนิดที่น่าสนใจ เช่น ดอกอัญชัญ ดอกเฟื่องฟ้า ดอกชบา ช้องนาง ขมิ้นชัน ใบเตย กะหล่ำปลีม่วง เปลือกมังคุด กระเจี๊ยบ เป็นต้น
ตารางที่ 1 ค่า pH ของอินดิเคเตอร์จากธรรมชาติ
|
ชนิดของพืช |
ช่วง pH ที่เปลี่ยนสี |
สีที่เปลี่ยน |
|
ดอกอัญชัน |
1-3 |
แดง-ม่วง |
|
ดอกกระเจี๊ยบ |
6-7 |
แดง-เขียว |
|
ขมิ้นชัน |
6-7 |
เหลืองส้ม |
|
ขมิ้นชัน |
11-12 |
ส้ม-น้ำตาล |
|
ชบาซ้อน |
7-8 |
แดง-เขียว |
|
ดาวเรืองเหลือง |
9-10 |
ไม่มีสี-เขียว |
|
กล้วยไม้ |
10-11 |
ไม่มีสี-เหลือง |
แหล่งที่มา
มหาวิทยาลัยมหิดล. Learning Science วิชาเคมี เรื่อง กรด-เบส. อินดิเคเตอร์สำหรับกรด-เบส: การเปลี่ยนสีของอินดิเคเตอร์. สืบค้นเมื่อวันที่ 20 ตุลาคม 2562. จาก https://il.mahidol.ac.th/e-media/acid-base/C8.HTM
รศ.ดร. ศุภจิตรา ชัชวาลย,ผศ.ดร. กนกวรรณ. เสรีภาพการทดลอง เรื่องสีสันแห่งธรรมชาติ.สืบค้นเมื่อวันที่ 20 ตุลาคม 2562. จาก https://www.enjoy-science.org/wp-content/uploads/2017/10/TCU_Book_2.pdf
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี. หนังสือแบบเรียนเคมีเพิ่มเติม เล่ม 4 ฉบับปรับปรุง พ.ศ. 2560. สารละลาย: การไทเทรตกรด-เบส. ศูนย์หนังสือจุฬาลงกรณ์มหาวิทยาลัย: กรุงเทพฯ
-
คำที่เกี่ยวข้อง



