ทำความเข้าใจกันใหม่ : น้ำ ไม่ได้นำไฟฟ้า
ทำความเข้าใจกันใหม่ : น้ำ ไม่ได้นำไฟฟ้า
อีกหนึ่งความเข้าใจผิด ที่คนจำนวนมากมักจะเข้าใจผิดกัน นั่นคือ สมบัติการนำไฟฟ้าของน้ำ อันเนื่องมาจากภาพลักษณ์ระหว่างน้ำกับไฟฟ้าที่ถูกนำเสนอออกมาตามสื่อต่างๆ ทำให้ง่ายต่อการเข้าใจผิด เช่น หากเล่นเกม ก็มีอยู่หลายเกมที่สร้างให้คุณสมบัติของธาตุน้ำ แพ้ทางต่อธาตุสายฟ้า หรือหากดูภาพยนตร์ ก็มีภาพยนตร์หลายเรื่องมิใช่น้อย ที่หากเกิดเหตุการณ์ที่ไฟรัวลงมาในจุดที่มีน้ำอยู่ จะทำให้เกิดเหตุอันตรายผู้คนถูกไฟดูดจำนวนมาก
ภาพลักษณ์ของน้ำและไฟฟ้าเมื่อมาคู่กันไฟฟ้านั้น ถูกมองว่าเป็นสิ่งที่อันตราย เชื่อว่าคนจำนวนมากกว่า 50% เข้าใจว่า น้ำ มีสมบัติการนำไฟฟ้า

ในบทความนี้ จะขอนำเสนอน้ำในภาพลักษณ์ที่ถูกต้องตามหลักทางวิทยาศาสตร์ว่าน้ำไม่ได้มีสมบัตินำไฟฟ้าด้วยตัวมันเองแต่อย่างใด แต่ก่อนที่จะอธิบายว่าทำไม น้ำจึงไม่ได้มีสมบัติการนำไฟฟ้า เรามารู้จักกันก่อนดีกว่าว่า สมบัตินำไฟฟ้าคืออะไร และเกิดขึ้นได้อย่างไร
กระแสไฟฟ้าเกิดจากการเคลื่อนที่ของประจุไฟฟ้า ซึ่งประจุไฟฟ้าสามารถเคลื่อนที่ได้ในตัวกลางหลายๆชนิด เรียกสมบัติของตัวกลางที่ยอมให้ประจุไฟฟ้าเคลื่อนที่ผ่านได้ว่า “ตัวนำไฟฟ้า” ขณะที่มีกระแสไฟฟ้าในตัวนำแสดงว่า “มีการนำไฟฟ้า”

การนำไฟฟ้าของสารละลาย
สารละลายที่นำไฟฟ้าได้เรียกว่า “สารละลายอิเล็กโทรไลต์(Electrolytic solution)” เช่น สารละลายกรดเกลือ
- ถ้านำไฟฟ้าได้มากเรียกว่า สารละลายอิเล็กโทรไลต์แก่ (strong electrolyte) เช่น สารละลายโซเดียมคลอไรด์
- ถ้านำไฟฟ้าได้น้อยเรียกว่า สารละลายอิเล็กโทรไลต์อ่อน(weak electrolyte) เช่น สารละลายกรดอะซิติก
- ถ้าเป็นสารละลายที่ไม่นำไฟฟ้าเรียกว่า “สารละลายนอนอิเล็กโทรไลต์ (Non-electrolytic solution)” เช่น สารละลายกลูโคส
การที่สารละลายอิเล็กโทรไลต์ นำไฟฟ้าได้ เพราะในสารละลายมีไอออนซึ่งมีประจุไฟฟ้าเรียกว่า ไอออนบวก และไอออนลบ กล่าวคือ
เมื่อสารละลายในน้ำจะมีการแตกตัวออกเป็นสองส่วน และมีประจุตรงกันข้ามกัน แต่ละส่วนเรียกว่า ไอออน
- ไอออนส่วนหนึ่งจะมีประจุไฟฟ้าบวก เรียกว่า ไอออนบวก
- ไอออนอีกส่วนหนึ่งจะมีประจุไฟฟ้าลบเรียกว่า ไอออนลบ (มีปริมาณเท่ากับไอออนบวก)
เมื่ออยู่ในสนามไฟฟ้า ไอออนบวกจะเคลื่อนที่เข้าหาขั้วไฟฟ้าลบ และ ไอออนลบจะเคลื่อนที่เข้าหาขั้วไฟฟ้าบวก ไอออนบวกที่เคลื่อนที่เข้าหาขั้วไฟฟ้าลบจะไปรับประจุลบหรืออิเล็กตรอน ส่วนไอออนลบที่เคลื่อนที่เข้าหาขั้วไฟฟ้าบวกจะเป็นตัวพาประจุลบไปให้ขั้วไฟฟ้า ไหลวนเวียนกันอยู่ในสารละลาย จึงก่อให้เกิดการนำไฟฟ้าขึ้น
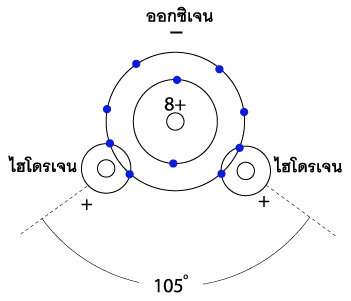
น้ำบริสุทธิ์ ไม่มีสี ไม่มีกลิ่น และไม่มีรส น้ำ 1 โมเลกุล (H2O) ประกอบด้วย ไฮโดรเจน 2 อะตอม และออกซิเจน 1 อะตอม เชื่อมต่อกันด้วยพันธะโควาเลนท์ (Covalent bonds) ซึ่งใช้อีเล็กตรอนร่วมกัน โดยที่อะตอมทั้งสามตัวเรียงกันทำมุม 105 องศา โดยมีออกซิเจนเป็นขั้วลบ และไฮโดรเจนเป็นขั้วบวก ดังรูปมากขึ้น
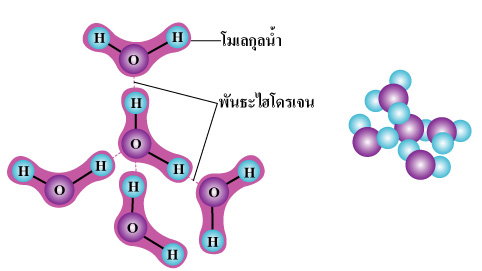
โมเลกุลแต่ละโมเลกุลของน้ำเชื่อมต่อกันด้วยพันธะไฮโดรเจน (Hydrogen-bonds) เรียงตัวต่อกันเป็นรูปจัตุรมุข (Tetrahedral) ดังรูปที่ 2 ทำให้น้ำต้องใช้ที่ว่างมากเมื่อเปลี่ยนสถานะเป็นน้ำแข็ง ดังนั้นเมื่อเราเพิ่มความร้อนให้กับก้อนน้ำแข็ง พันธะไฮโดรเจนที่เชื่อมระหว่างโมเลกุลจะถูกทำลาย (พันธะโควาเลนท์มีความแข็งแกร่งกว่าพันธะไฮโดรเจน) ทำให้น้ำแข็งละลายเป็นของเหลว โครงสร้างผลึกยุบตัวลง น้ำในสถานะของเหลวจึงใช้เนื้อที่น้อยกว่าน้ำแข็ง นี่เองคือ สาเหตุว่าทำไมน้ำแข็งจึงมีความหนาแน่นต่ำกว่าน้ำ
ตัวอย่างที่แสดงพันธะไฮโดรเจนที่เห็นได้ชัดคือ แรงตรึงผิวของน้ำ (Surface tension) เราจะเห็นว่า หยดน้ำบนพื้น หรือบนใบบัว จะเป็นทรงกลมคล้ายเลนส์นูน หรือเวลาที่เติมน้ำให้เต็มแก้ว น้ำจะพูนโค้งอยู่สูงเหนือปากแก้วเล็กน้อย หากปราศจากแรงตรึงผิวซึ่งเกิดจากพันธะไฮโดรเจนแล้ว น้ำจะเต็มเรียบเสมอปากแก้วพอดี ไม่มีการนูน แรงตรึงผิวเป็นคุณสมบัติพิเศษของน้ำ ซึ่งมีมากกว่าของเหลวชนิดอื่น ยกเว้นปรอท (Mercury) ซึ่งเป็นธาตุชนิดเดียวที่เป็นของเหลว แรงตรึงผิวทำให้น้ำเกาะรวมตัวกัน และไหลชอนไชไปได้ทุกหนแห่ง แม้แต่รูโหว่และรอยแตกของหิน
สภาพการนำไฟฟ้าของน้ำ
ตามปกติแล้ว น้ำบริสุทธิ์จะไม่มีการเหนี่ยวนำไฟฟ้า การนำไฟฟ้าของน้ำแสดงถึง การเจือปนของสารละลายในน้ำ
การนำไฟฟ้า (Electrical Conductivity) ของน้ำประมาณการจำนวนของของแข็งที่ละลายในน้ำหรือ TDS ซึ่งย่อมาจากของแข็งละลายทั้งหมด TDS มีหน่วยวัดเป็น ppm (ส่วนในล้านส่วน) หรือ mg / l
ปัจจัยที่มีผลการนำไฟฟ้าของน้ำ การนำไฟฟ้าของน้ำขึ้นอยู่กับอุณหภูมิของน้ำ: สูงกว่าอุณหภูมิที่สูงกว่าการนำไฟฟ้าจะเป็น การนำไฟฟ้าของน้ำเพิ่มขึ้น 2-3% เพิ่มขึ้น 1 องศาเซลเซียสอุณหภูมิน้ำ EC เมตรจำนวนมากในปัจจุบันโดยอัตโนมัติมาตรฐานการอ่านเพื่อ 25C ในขณะที่การนำไฟฟ้าเป็นตัวบ่งชี้ที่ดีของความเค็มรวมก็ยังไม่ได้ให้ข้อมูลเกี่ยวกับองค์ประกอบของไอออนในน้ำใดๆ ค่าการนำไฟฟ้าเดียวกันสามารถวัดได้ในน้ำที่มีคุณภาพต่ำ (เช่นน้ำที่อุดมไปด้วยโซเดียมโบรอนและฟลูออไร) เช่นเดียวกับในน้ำชลประทานที่มีคุณภาพสูง (เช่นน้ำปฏิสนธิเพียงพอกับความเข้มข้นของสารอาหารที่เหมาะสมและอัตราส่วน)
หน่วยของการวัดของการนำไฟฟ้าของน้ำ
หน่วยที่ใช้กันทั่วไปสำหรับการวัดค่าการนำไฟฟ้าของน้ำ: ไมโครวินาที / cm (microsiemens / เซนติเมตร) หรือ dS / m (deciSiemens / m) ที่ไหน: 1,000 ไมโครวินาที / cm = 1 dS / m
ค่า TDS และค่า EC การนำไฟฟ้า
ตั้งแต่การนำไฟฟ้าเป็นตัวชี้วัดถึงความจุของน้ำที่จะดำเนินการกระแสไฟฟ้าก็จะเกี่ยวข้องโดยตรงกับความเข้มข้นของเกลือละลายในน้ำและดังนั้นจึงจะละลายของแข็งทั้งหมด (TDS) เกลือละลายเข้าไอออนประจุบวกและไอออนประจุลบซึ่งเป็นตัวนำไฟฟ้า เพราะมันเป็นเรื่องยากที่จะวัดค่า TDS ในสนามการนำไฟฟ้าของน้ำที่ถูกนำมาใช้เป็นตัวชี้วัด การนำไฟฟ้าของน้ำที่สามารถกำหนดได้ในวิธีที่รวดเร็วและราคาไม่แพงโดยใช้เมตรแบบพกพาน้ำกลั่นไม่ได้มีเกลือละลายและเป็นผลก็ไม่ได้ดำเนินการผลิตไฟฟ้าและมีการนำไฟฟ้าของศูนย์ แต่เมื่อความเข้มข้นของเกลือถึงระดับหนึ่งการนำไฟฟ้าจะไม่เกี่ยวข้องโดยตรงกับความเข้มข้นของเกลือ เพราะนี่คือคู่ไอออนที่เกิดขึ้น คู่ไอออนลดลงค่าใช้จ่ายของแต่ละคนเพื่อให้เหนือระดับนี้ TDS ที่สูงขึ้นจะไม่ส่งผลให้การนำไฟฟ้าที่สูงขึ้นอย่างเท่าเทียมกัน
EC สามารถแปลงเป็น TDS ใช้คำนวณดังนี้
TDS (ppm) = 0.64 x EC (ไมโครวินาที / ซม.) = 640 x EC (dS / m)
การนำไฟฟ้าของน้ำบริสุทธิ์
น้ำบริสุทธิ์ไม่ได้เป็นตัวนำไฟฟ้าที่ดี น้ำกลั่นสามัญในภาวะสมดุลกับก๊าซคาร์บอนไดออกไซด์ในอากาศมีการนำประมาณ 10 x 10-6 W-1 * เมตร-1 (20 dS / m) เพราะกระแสไฟฟ้าจะถูกส่งโดยไอออนในการแก้ปัญหาการเพิ่มขึ้นของการนำความเข้มข้นของการเพิ่มขึ้นของไอออน
การนำไฟฟ้าของน้ำทั่วไป:
- น้ำบริสุทธิ์นำไฟฟ้า · 10-6 S / m
- น้ำดื่มนำไฟฟ้า 0.005-0.05 S / m
- น้ำทะเลนำไฟฟ้า 5 S / m
ทั้งจากสมบัติพื้นฐาน และจากการทดลอง จะเห็นว่าหากเราพิจารณา เฉพาะน้ำ บริสุทธิ์ ในความเป็นจริงแล้วนั้น น้ำบริสุทธิ์สามารถนำๆฟฟ้าได้น้อยมากๆ หรือเรียกได้ว่า ไม่มีคุณสมบัติการนำไฟฟ้าเลยก็ว่าได้ แต่ที่เราเห็นว่าน้ำสามารถนำไฟฟ้าได้ เป็นผลเนื่องมาจากสิ่งเจอปนที่อยู่ในน้ำเท่านั้นเอง
เนื้อหาจาก
http://www.grendelschildren.com/
http://www.mssti.com/
http://webhtml.horhook.com/wbi/ec/2conductors-02.htm
http://www.geocities.ws/chemonline2000/modelatom/__7.html
http://portal.edu.chula.ac.th/lesa_cd/assets/document/lesa212/7/properties_water/properties_water/properties_water.html
http://nakhamwit.ac.th/pingpong_web/m&c_web/Content_03.html
https://sites.google.com/site/sarlaeasmbatikhxngsa/reuxng-thi-3-karna-fifa-laea-karna-khwam-rxn-khxng-sar
https://physicskruadd.wordpress.com/2012/03/13/
ภาพจาก
http://portal.edu.chula.ac.th/lesa_cd/assets/document/lesa212/7/properties_water/properties_water/properties_water.html
https://commons.wikimedia.org/wiki/File:Electric_water_valve_water_effect.jpg
http://www.gizmodo.com.au/2015/11/how-will-electricity-work-in-2115/



