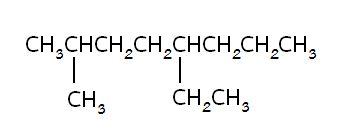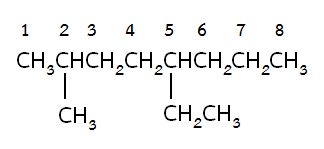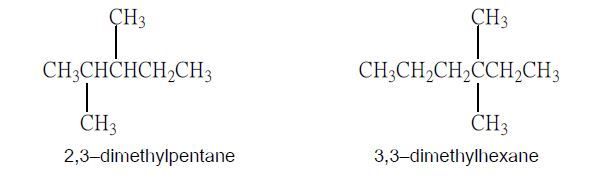สารประกอบไฮโดรคาร์บอนอิ่มตัว
สารประกอบไฮโดรคาร์บอน ( Hydrocarbon Compounds ) คือสารประกอบที่มีเฉพาะคาร์บอนและไฮโดรเจนเป็นองค์ประกอบ ไฮโดรคาร์บอนส่วนใหญ่เกิดตามธรรมชาติ อาทิ น้ำมันดิบ ถ่านหิน ปิโตรเลียม ยางไม้ เป็นต้น สามารถแบ่งออกได้เป็น 2 ประเภทใหญ่ๆ ตามชนิดของพันธะ ได้แก่
-
สารประกอบไฮโดรคาร์บอนอิ่มตัว ( Saturated Hydrocarbons ) ได้แก่ แอลเคน ( Alkanes ) และ ไซโคลแอลเคน ( Cycloalkanes )
-
สารประกอบไฮโดรคาร์บอนไม่อิ่มตัว ( Unsaturated Hydrocarbons ) ได้แก่ แอลคีน ( Alkenes ) และ ไซโคลแอลคีน ( Cycloalkenes ) แอลไคน์ ( Alkynes ) และอะโรมาติกไฮโดรคาร์บอน ( Aromatic Hydrocarbons )

ภาพแก๊สผสมระหว่างโพรเพนกับบิวเทนในเป็นเชื้อเพลิงหุงต้มในครัวเรือน
ที่มา: https://pixabay.com, Magnascan
ซึ่งในบทนี้ผู้เขียนจะขอกล่าวถึงสารประกอบไฮโดรคาร์บอนอิ่มตัว ในรายละเอียดเกี่ยวกับการเรียกชื่อ คุณสมบัติของสาร รวมถึงการใช้ประโยชน์ ของสารประกอบไฮโดรคาร์บอนอิ่มตัว
สารประกอบไฮโดรคาร์บอนอิ่มตัว เป็นสารประกอบไฮโดรคาร์บอนที่พันธะระหว่างคาร์บอนอะตอมในโมเลกุลเป็นพันธะเดี่ยวทั้งหมด มีทั้งโครงสร้างที่เป็นโซ่เปิดและโซ่กิ่ง เรียกว่า แอลเคน และโครงสร้างที่เป็นโซ่ปิด เรียกว่า ไซโคลแอลเคน สารประกอบพวกนี้มีทั้งที่เกิดในธรรมชาติ เช่น น้ำมันดิบ น้ำมันปิโตรเลียม ก๊าซธรรมชาติ นอกจากนี้ยังสามารถสังเคราะห์ขึ้นมาได้ ตัวแรกของอนุกรมแอลเคน คือ มีเทน
การเรียกชื่อสารประกอบแอลเคน
สารประกอบแอลเคน มีวิธีการเรียกชื่อตามระบบ IUPAC ( International Union of Pure and Applied Chemistry ) ได้โดยใช้จำนวนนับในภาษากรีกระบุจำนวนอะตอมของคาร์บอน และลงท้าย ด้วย เ –น ( -ane ) จำนวนนับภาษากรีกมีดังนี้
1 = มีท หรือ เมท ( meth- ) 6 = เฮกซ ( hex- )
2 = อีท หรือ เอท ( eth- ) 7 = เฮปท ( hept- )
3 = โพรพ ( prop- ) 8 = ออกท ( oct- )
4 = บิวท ( but- ) 9 = โนน ( non- )
5 = เพนท ( pent- ) 10 = เดกค ( deca- )
และมีขั้นตอนในการเรียกดังนี้
-
เลือกโซ่คาร์บอนที่ยาวที่สุดเป็นโซ่หลัก ( parent name ) เช่น
จากสูตรโครงสร้างข้างบนจะเห็นได้ว่าโซ่คาร์บอนที่ยาวที่สุดมีคาร์บอนต่อกัน 8 อะตอม จึงเรียกชื่อโซ่หลักว่า ออกเทน ( octane )
-
กำหนดตำแหน่งของคาร์บอนอะตอมในโซ่หลัก โดยให้ตำแหน่งของคาร์บอนที่มีหมู่แทนที่ ( substituent ) มีตัวเลขต่ำสุด เช่น
จากสูตรโครงสร้างข้างบนถ้านับจากขวาไปซ้ายจะทำให้หมู่แทนที่อยู่ที่ตำแหน่งที่ 4 และ 7 แต่ถ้านับจากซ้ายไปขวา หมู่แทนที่จะอยู่ที่ตำแหน่งที่ 2 และ 5 ดังนั้นจึงนับจากซ้ายไปขวาเพราะตัวเลขของหมู่แทนที่จะต่ำกว่า
-
หมู่แทนที่ต่ออยู่กับตำแหน่งใดของคาร์บอนอะตอมในโซ่หลักการอ่านชื่อก็จะระบุตำแหน่งของคาร์บอนอะตอมนั้นแล้วตามด้วยชื่อของหมู่แทนที่ โดยจำนวนคาร์บอนของหมู่แทนที่จะลงท้ายด้วย อิล เช่น ในตัวอย่างข้างต้นอ่านว่าหมู่ 2–methyl และ 5–ethyl ตามลำดับ
-
ในการเรียกชื่อจะเริ่มด้วยชื่อของหมู่แทนที่เรียงตามลาดับตัวอักษรแล้วตามด้วยชื่อหลัก ดังนั้นสารประกอบในตัวอย่างข้างต้นจึงมีชื่อเรียกว่า 5–ethyl - 2–methyloctane
-
ถ้าในโมเลกุลมีหมู่แทนที่ชนิดเดียวกันมากกว่า 1 หมู่ ให้เติมคำบอกจำนวนหมู่ด้วยภาษาละตินเพื่อบอกถึงจำนวนของหมู่แทนที่ ดังนี้
di = 2 tri = 3 tetra = 4
penta = 5 hexa = 6 hepta = 7
octa = 8 nona = 9 deca = 10
และถ้าหมู่แทนที่ชนิดเดียวกันแทนที่อยู่ที่คาร์บอนอะตอมเดียวกันทั้ง 2 หมู่ให้ระบุตัวเลขของตำแหน่งนั้นซ้ำ เช่น
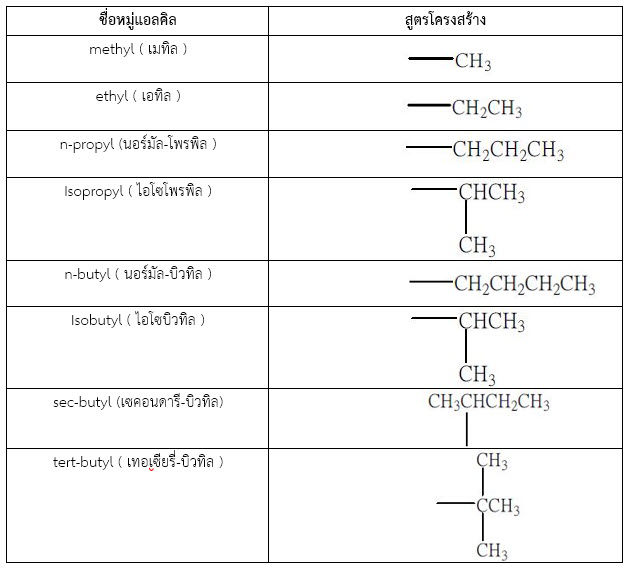
- สำหรับหมู่แอลคิล ( alkyl group ) ซึ่งเป็นหมู่แทนที่นั้น เกิดจากการลดจำนวนอะตอมของ ไฮโดรเจนในแอลเคนลง 1 อะตอม จึงมีสูตรทั่วไป CnH2n+1 ตัวอย่างหมู่แอลคิลที่สำคัญมีรายละเอียดดังตารางต่อไปนี้
ตารางที่ 1. แสดงชื่อและสูตรโครงสร้างหมู่แอลคิลที่สำคัญ
การเรียกชื่อสารประกอบไซโคลแอลเคน
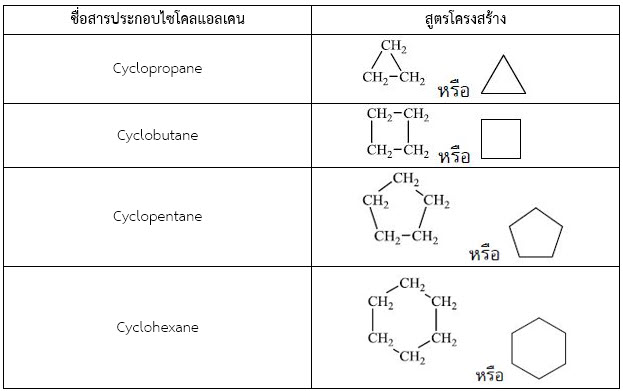
การเรียกชื่อไซโคลแอลเคนจะเรียกทำนองเดียวกับแอลเคน ยกเว้นแต่ชื่อหลักซึ่งบอกจำนวนคาร์บอนในวงนั้นจะต้องนำหน้าด้วยคา ว่า ไซโคล ( cyclo- ) ซึ่งแสดงดังตาราง
ตารางที่ 2. แสดงชื่อและสูตรโครงสร้างของสารประกอบไซโคลแอลเคนบางชนิด
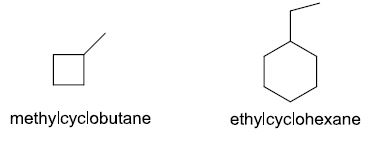
ไซโคลแอลเคนที่มีหมู่แอลคิลแทนที่จะเรียกชื่อเป็นอนุพันธ์ของไซโคลแอลเคน โดยถ้ามีการแทนที่เพียง 1 หมู่ ก็ไม่จำเป็นต้องระบุตำแหน่งที่แทนที่ เพราะทุก ๆ ตำแหน่งในวงจะสมมาตร
กันหมด เช่น
แต่ถ้ามีการแทนที่ตั้งแต่ 2 ตำแหน่งขึ้นไป จาเป็นต้องระบุตำแหน่งที่มีการแทนที่ด้วย โดยทั่วไปให้มีการนับตำแหน่งที่มีการแทนที่ใด ๆ เป็นตำแหน่งที่ 1 แล้วนับวนไปจนรอบวงในทิศทางที่ทำ ให้หมู่แทนที่มีตัวเลขน้อยที่สุด เช่น
คุณสมบัติบางประการของสารประกอบแอลเคนและไซโคลแอลเคน
-
แอลเคนไม่ละลายน้ำซึ่งเป็นโมเลกุลที่มีขั้ว และลอยอยู่ชั้นบนเพราะมีความหนาแน่นน้อยกว่าน้ำ ละลายได้บางส่วนในแอลกอฮอล์ และละลายได้ดีในโทลูอีนซึ่งเป็นโมเลกุลไม่มีขั้ว
-
แอลเคนและไซโคลแอลเคนไม่มีหมู่ฟังก์ชันในโมเลกุลจึงเป็นสารที่เฉื่อย ( inert ) ต่อปฏิกิริยาเคมี
-
จุดเดือดจุดหลอมเหลวสูงขึ้นตามจำนวนคาร์บอนที่เพิ่มขึ้น และไซโคลแอลเคนจะมีจุดเดือดจุดหลอมเหลวสูงกว่าแอลเคนที่มีคาร์บอนเท่ากัน
-
ที่อุณหภูมิห้อง แอลเคนที่มี C 1-4 อะตอม เป็นแก๊ส 5–17 อะตอม เป็นของเหลว และ 18 อะตอมขึ้นไปเป็นของแข็ง
-
แอลเคนและไซโคลแอลเคนเป็นสารประกอบไฮโดรคาร์บอนที่มีพันธะเดี่ยวหมดจัดเป็นสารประกอบคาร์บอนประเภทอิ่มตัว สามารถเกิดปฏิกิริยาแทนที่กับเฮโลเจนในที่มีแสงสว่าง ติดไฟได้ดีไม่มีเขม่าและควัน
ประโยชน์และโทษของสารประกอบแอลเคนและไซโคลแอลเคน
-
มีเทนใช้เป็นเชื้อเพลิงในโรงงานไฟฟ้า โรงงานต่าง ๆ และใช้เป็นวัตถุดิบในการผลิตเคมีภัณฑ์ต่าง ๆ เช่น เมทานอล อีเทน และโพรเพน นอกจากนี้ ยังใช้กับรถยนต์ เรียกว่าแก๊ส NGV ( Natural Gas for Vehicle )
-
อีเทน ( C2H6 ) และโพรเพน ( C3H8 ) ใช้ในการผลิตเอทิลีน ( C2H4 ) และโพรพิลีน ( C3H6 ) เพื่อเป็นสารตั้งต้นในการผลิตเม็ดพลาสติก
-
แก๊สผสมระหว่างโพรเพน ( C3H8 ) กับบิวเทน ( C4H10 ) ใช้เป็นแก๊สเชื้อเพลิงหุงต้ม แก๊สทั้งสองได้จากการกลั่นปิโตรเลียมและแก๊สธรรมชาติ เมื่อบรรจุในถังเหล็กภายใต้ความดันสูง จะมีสถานะเป็นของเหลว จึงเรียกว่า “แก๊สปิโตรเลียมเหลว” ( Liquefied Petroleum Gas หรือ LPG )
-
เฮกเซน ใช้เป็นตัวทำละลายในอุตสาหกรรมการสกัดน้ำมันพืช และน้ำหอม
-
ไซโคลเฮกเซน ใช้เป็นตัวทำละลายในการทำเรซินและแลกเกอร์ ใช้ล้างสี ใช้เป็นสารตั้งต้นในการผลิตสารประกอบอินทรีย์ เช่น เบนซีน
-
แอลเคนน้ำหนักโมเลกุลสูง เช่น พาราฟิน ใช้เคลือบผลไม้เพื่อรักษาความชุ่มชื้นและยับยั้งการเจริญเติบโตของเชื้อรา นอกจากนี้ ยังใช้แอลเคนเป็นสารตั้งต้นในอุตสาหกรรมหลายชนิด ได้แก่ อุตสาหกรรมสารซักฟอก เส้นใย สารเคมีทางการเกษตรและยาปราบศัตรูพืช
นอกจากจะมีประโยชน์แล้ว แอลเคนก็มีโทษเช่นเดียวกัน เนื่องจากสามารถละลายสารอินทรีย์ไม่มีขั้วอย่างพวกไขมันและน้ำมันได้ เมื่อสูดดมไอของแอลเคนเข้าไปจะทำให้เป็นอันตรายกับเนื้อเยื่อปอด เพราะไปละลายไขมันในผนังเซลล์ที่ปอด นอกจากนี้แอลเคนบางชนิดที่ใช้เป็นตัวทำละลาย เช่น เอกเซน ทำให้ผิวหนังแห้งเจ็บ คันและแตก เพราะไปละลายน้ำมันที่ผิวหนัง ทำให้ผิวหนังขาดความชุ่มชื้นจึงแห้งและแตก
แหล่งที่มา
กิตติ ปวนกาศ. สารประกอบอัลเคน. สืบค้นเมื่อวันที่ 4 มีนาคม 2562 . จาก https://oriokitti.wordpress.com/เนื้อหาบทเรียน/สารประกอบอัลเคน-alkanes/
อินทิรา หาญพงษ์พันธ์ และคณะ. เคมีอินทรีย์. สืบค้นเมื่อวันที่ 4 มีนาคม 2562. จาก https://www.slideshare.net/firsthihi/chemistry-11225866
DLIT Resources คลังสื่อการสอน. การทำปฏิกิริยาระหว่างสารประกอบไฮโดรคาร์บอนกับสารละลายโบรมีน. สืบค้นเมื่อวันที่ 4 มีนาคม 2562 จาก https://www.youtube.com/watch?v=FTImsZcLBLU