อะตอมและตารางธาตุ 1
การค้นพบอะตอม

ภาพ บทเรียนเรื่อง อะตอมและตาราธาตุ
ที่มา อนุสิษฐ์ เกื้อกูล
ความคิดที่ว่าสารทั้งปวงประกอบด้วยส่วนประกอบพื้นฐานชนิดหนึ่ง ได้เริ่มขึ้นในศตวรรษที่ 5 ก่อนคริสต์ศักราชเมื่อลิวคิปปอส (Leukippos) และดีมอคริตอส (Demokritos) เสนอทฤษฎีที่กล่าวถึงอะตอม(atom) (โดยคำว่า atom มาจากภาษากรีกว่า atomos a แปลว่า ไม่ tomos แปลว่า แบ่งได้) และอธิบายว่าการที่สารต่างชนิดกันมีสมบัติต่างกันนั้นเป็นเพราะอะตอมของสารเหล่านั้นมีรูปร่าง น้ำหนัก การจัดตัวและการรวมตัวไม่เหมือนกัน ตัวอย่างเช่น อะตอมของของเหลว มีรูปร่างกลมเรียบและสามารถกลิ้งไปมาได้ง่าย ในขณะที่อะตอมของของแข็งจะมีรูปขรุขระ ซึ่งสามารถเกาะกันได้ดีกว่า

Democritos (460-370 BC)
ที่มา https://geoffneilsen.wordpress.com/navigation/beginings/democritus-of-abdera-c-460-c-370-bc/
Demokritos ใช้วิธีการสังเกตว่าสสารมีการเปลี่ยนแปลงอย่างไรโดยเขาเชื่อว่าการเคลื่อนที่ของอะตอมเป็นสาเหตุทำให้เกิดการเปลี่ยนแปลงของสาร อย่างไรก็ตาม Demokritos ไม่ได้มีหลักฐานแสดงให้เห็นว่าทฤษฎีของเขาถูกต้องอย่างไรก็ตามมีเพียงบุคคลบางกลุ่มที่เห็นด้วยกับทฤษฎีของDemokritos

Dalton (1766 - 1844)
ที่มา https://en.wikipedia.org/wiki/John_Dalton
ในระหว่างศตวรรษที่ 17 และ 18 เป็นจุดเริ่มต้นของการศึกษาเรื่อง สสารอย่างเป็นระบบและมีการพัฒนาวิทยาศาสตร์มากขึ้นโดยเฉพาะในยุโรป ช่วงนี้มีผู้ค้นพบและพัฒนาทฤษฎีทางวิทยาศาสตร์จำนวนมาก หนึ่งในนั้นคือ จอห์น ดอลตัน ซึ่งเป็นนักเคมี นักอุตุนิยมวิทยา จอห์น ดอลตัน เกิดในตระกูลชาวนาและช่างทอผ้าในอังกฤษ เขาเป็นนักเรียนที่ฉลาดและแก้ปัญหาทางคณิตศาสตร์ได้อย่างรวดเร็ว เมื่อเขาจบการศึกษาได้ทำงานเป็นเลขานุการของ Manchester Literary และ Philosophical Society และเขาเริ่มศึกษาพฤติกรรมของแก๊สอย่างจริงจังและเป็นระบบ โดยเริ่มต้นด้วยการศึกษาองค์ประกอบของแก๊สผสม ความดันของไอน้ำและไออื่นๆ ที่อุณหภูมิแตกต่างกัน จากการทดลองของเขาหลายครั้งทำให้เขาสามารถตั้งทฤษฎีของแก๊ส โดยเฉพาะเรื่องความดันย่อยของแก๊ส จนเกิดเป็นกฏความดันย่อยของดอลตัน ในปี คศ.1803 ดอลตันทำการทดลองและเก็บข้อมูลเกี่ยวกับแก๊สและการเกิดสารประกอบอีกหลายประเด็น จนทำให้เขาสามารถนำไปสู่การตั้งทฤษฎีอะตอมเพื่อใช้อธิบายเกี่ยวกับการเปลี่ยนแปลงมวลของสารก่อนและหลังทำปฏิกิริยา รวมทั้งอัตราส่วนโดยมวลของธาตุที่รวมกันเป็นสารประกอบหนึ่งๆ ซึ่งมีสาระสำคัญดังนี้
1.ธาตุประกอบด้วยอนุภาคเล็กๆ หลายอนุภาคอนุภาคเหล่านี้เรียกว่า อะตอม ซึ่งแบ่งแยกและทำให้สูญหายไม่ได้
2.อะตอมของธาตุชนิดเดียวกันมีสมบัติเหมือนกัน เช่น มีมวลเท่ากัน แต่จะมีสมบัติแตกต่างจากอะตอมของธาตุอื่น
3.สารประกอบเกิดจากอะตอมของธาตุมากกว่าหนึ่งชนิดทำปฏิกิริยาเคมีกันในอัตราส่วนที่เป็นเลขลงตัวน้อยๆ
4.โมเลกุลของสารประกอบชนิดเดียวกันย่อมมีสมบัติเหมือนกันทุกประการ และมีสมบัติแตกต่างจากสารประกอบอื่น
ทฤษฎีอะตอมของดอลตันช่วยให้นักวิทยาศาสตร์ในสมัยนั้นสามารถอธิบายลักษณะและสมบัติของอะตอมได้เพียงระดับหนึ่ง ต่อมาได้มีการศึกษาเกี่ยวกับอะตอมเพิ่มขึ้นและค้นพบข้อมูลบางประการที่ไม่สอดคล้องกับแนวคิดของดอลตัน เช่น พบว่าอะตอมของธาตุชนิดเดียวกันอาจมีมวลแตกต่างกันได้ อะตอมสามารถแบ่งแยกได้ นักวิทยาศาสตร์รุ่นต่อมาจึงได้ศึกษาเพิ่มเติมแล้วสร้างแบบจำลองอะตอมขึ้นมาใหม่

แบบจำลองอะตอมของดอลตัน
ที่มา อนุสิษฐ์ เกื้อกูล
กลับไปที่เนื้อหา
สมบัติของหลอดรังสีแคโทด
Sir Joseph John Thomson นักวิทยาศาสตร์ชาวอังกฤษได้รวบรวมนำการทดลองของสาขาต่างๆ เช่น การทดลองการนำไฟฟ้าของแก๊สโดยใช้หลอดรังสีแคโทด การหาค่าประจุของอิเล็กตรอนโดยวิธีหยดน้ำมันของมิลลิแกน มาสนับสนุนแบบจำลองอะตอมที่ได้นำเสนอขึ้นโดยมีลำดับการศึกษาดังนี้
การศึกษาของ William Crooks
นักวิทยาศาสตร์ได้ทดลองการนำไฟฟ้าของแก๊ส โดยผ่านกระแสไฟฟ้าเข้าไปในแก๊สที่มีความดันต่างๆ กันพบว่า ที่ความดันปกติ1 บรรยากาศ อากาศและแก๊สต่างๆ จะไม่นำไฟฟ้า แต่ถ้าลดความดันของแก๊สให้ต่ำลงและเพิ่มความต่างศักย์ระหว่างขั้วไฟฟ้าให้มากขึ้น แก๊สจะนำไฟฟ้าได้ดี(ปรากฏการณ์ธรรมชาติที่แสดงว่าแก๊สนำไฟฟ้าได้คือ การเกิดฟ้าผ่า
William Crooks ได้ประดิษฐ์อุปกรณ์เพื่อศึกษาการนำไฟฟ้าของแก๊สซึ่งประกอบด้วยหลอดแก้วที่บรรจุแก๊สที่ความดันต่ำ มีขั้วไฟฟ้าเป็นแผ่นโลหะ 2 ขั้วต่อเข้ากับเครื่องกำเนิดไฟฟ้าที่มีความต่างศักย์สูง(10,000-20,000 โวลต์) และยังวางฉากเรืองแสง(ZnS ซิงค์ซัลไฟด์) ขนาดหลอดตามแนวยาว ดังรูปที่ 1
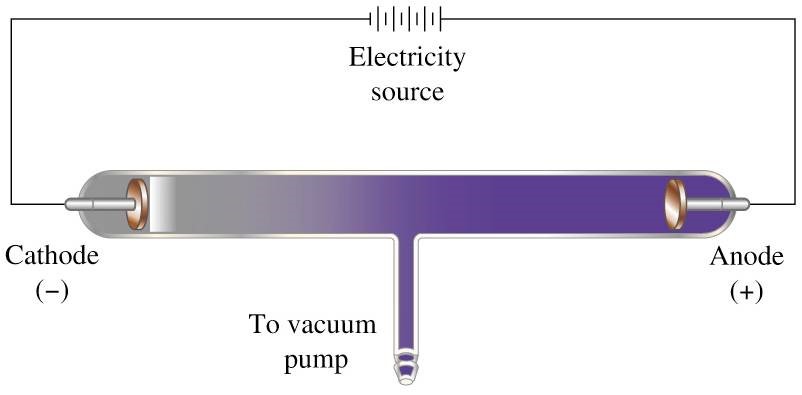
ภาพหลอดรังสีแคโทดของ William Crookes
ที่มา https://sites.google.com/site/khemikhrupanpan/bth-thi1/william-crookes
จากผลการทดลองของ Crookes พบว่า
1.ที่ความดัน 1 บรรยากาศ ไม่เห็นการเปลี่ยนแปลงใด
2.เมื่อลดความดันลงแก๊สภายในหลอดแก้วจะเรืองแสง
3.เมื่อลดความดันลงมากๆ บริเวณแอโนดจะเรืองแสง
4.เมื่อนำกังหันหมุนได้ไปไว้ระหว่างขั้วแอโนดและแคโทดใบพัดจะหมุนได้
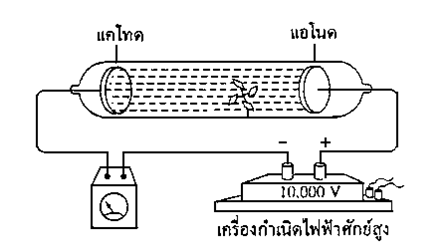
ภาพแสดงรังสีแคโทดทำให้ใบพัดของกังหันหมุนได้
ที่มา https://sites.google.com/site/khemikhrupanpan/bth-thi1/william-crookes
5.เมื่อนำฉากเรืองแสง ZnS ไว้ระหว่างขั้วแอโนดและแคโทดฉากด้านที่หันไปทางขั้วแคโทดจะ เรืองแสงและเกิดเงา
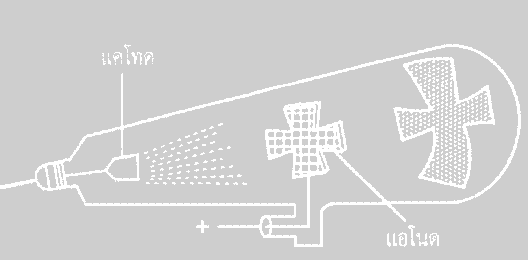
รูปที่ 3 แสดงการเกิดเงาเมื่อนำฉากเรืองแสงไว้ระหว่างขั้วแอโนดและแคโทด
ที่มา https://sites.google.com/site/khemikhrupanpan/bth-thi1/william-crookes
ดังนั้นเราจึงเรียกรังสีที่พุ่งออกมาจากขั้วแคโทดเป็นเส้นตรงมายังขั้วแอโนดว่า รังสีเคโทด ซึ่งรังสีดังกล่าวมีมวลเพราะทำให้ใบพัดหมุนได้และเรียกหลอดแก้วชนิดนี้ว่า หลอดรังสีแคโทด
กลับไปที่เนื้อหา
การทดลองหลอดรังสีแคโทดของ Sir Joseph John Thomson
ค.ศ. 1897 (พ.ศ.2440) Sir Joseph Jhon Thomson นักวิทยาศาสตร์ชาวอังกฤษ สนใจปรากฏการณ์ ทำการทดลองบรรจุแก๊สชนิดหนึ่งไว้ในหลอดแก้วที่ต่อไว้กับเครื่องสูบอากาศเพื่อลดความดันภายในหลอด ที่แอโนดเจาะรูตรงกลางและต่อไว้กับเครื่องกำเนิดไฟฟ้ากระแสตรงศักย์สูง ที่ปลายหลอดมีฉากเรืองแสงขวางอยู่ ดังรูปที่ 3 พบว่าเมื่อลดความดันในหลอดแก้วให้ต่ำลงมากๆ จนเกือบเป็นสุญญากาศ จะมีจุดสว่างเกิดขึ้นตรงบริเวณศูนย์กลางของฉากเรืองแสง
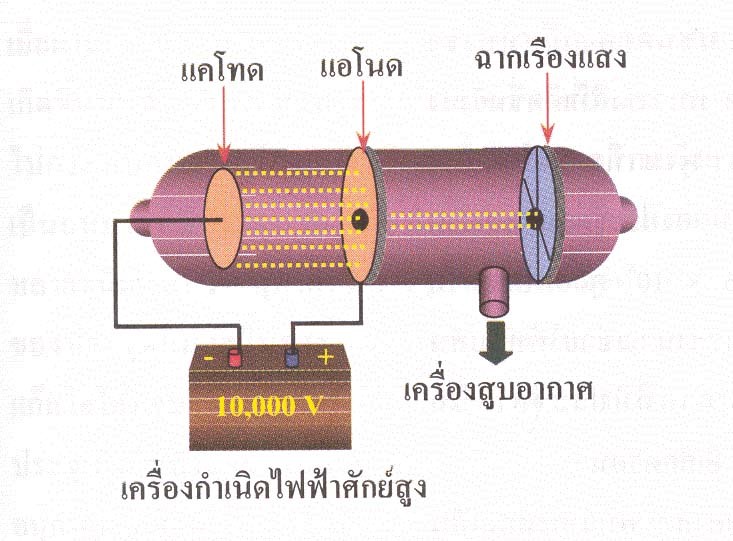
ภาพหลอดรังสีแคโทดที่ดัดแปลงแล้ว
ที่มา http://komsan1022.blogspot.com/
ผลการทดลองเป็นดังนี้
1.เมื่อลดความดันในหลอดแก้วให้ต่ำลงมากๆ จนเกือบเป็นสุญญากาศจะมีจุดสว่างเกิดขึ้นบนฉากเรืองแสง ทอมสันจึงตั้งสมมติฐานว่า มีรังสีชนิดหนึ่งพุ่งเป็นเส้นตรงมาจากแคโทดไปกระทบฉากเรืองแสง(ศึกษาหลอดรังสีแคโทด) แต่ไม่ทราบว่าเป็นอนุภาคชนิดใด จากผลการทดลองนี้เอง ทอมสันเชื่อว่าอะตอมไม่ใช่ทรงกลมตันตามแบบจำลองอะตอมของดอลตัน เพราะว่าถ้าเป็นทรงกลมตันจริงจะต้องไม่มีรังสีพุ่งมาชนที่ฉากเรืองแสง
2.สมมติฐานของทอมสันที่ว่ามีอนุภาคที่มีประจุเกิดขึ้น ทอมสันได้ทดลองต่อโดยอาศัยหลักการที่ว่าถ้ามีอนุภาคที่มีประจุจริง อนุภาคนั้นต้องเบี่ยงเบนในสนามไฟฟ้าและสนามแม่เหล็ก
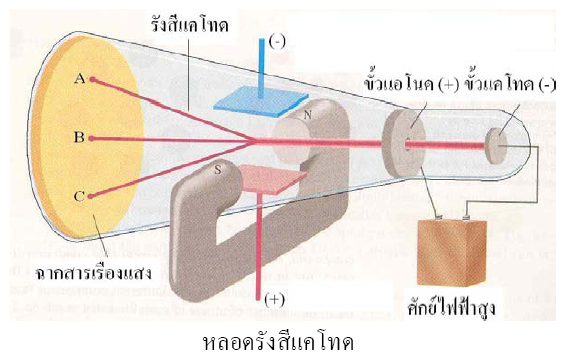
ภาพแสดงการเบี่ยงเบนของอนุภาคในสนามไฟฟ้าและสนามแม่เหล็ก
ที่มา https://sites.google.com/site/phiraporn05/khorngsrang-xatxm-1
จากรูปเมื่อนำสนามไฟฟ้าภายนอกมากระทำต่อรังสีแคโทด พบว่ารังสีแคโทดจะเบนออกจากตำแหน่งเดิม คือเบี่ยงเบนเข้าหาขั้วบวกของสนามไฟฟ้า ที่จุด C แสดงว่าอนุภาคนั้นควรมีประจุ
เมื่อนำสนามแม่เหล็กมาไว้แทนสนามไฟฟ้าภายนอก อนุภาคที่มีประจุลบจะเคลื่อนที่เบี่ยงเบนไปจากตำแหน่งเดิมในทิศทางตรงกันข้ามกับการเบี่ยงเบนในสนามไฟฟ้าภายนอก ที่จุด A
เมื่อทดลองถึงตอนนี้ ทอมสันอยากทราบว่าอนุภาคลบนี้เกิดจากส่วนของโลหะที่ทำแคโทดหรือเกิดจากแก๊สที่บรรจุอยู่ภายในหลอดรังสีแคโทด
3.เมื่อทอมสันทดลองเปลี่ยนแก๊สชนิดต่างๆ มาบรรจุภายในหลอดรังสีแคโทด โดยใช้โลหะที่ทำแคโทดชนิดเดิม ปรากฏว่าผลการทดลองเหมือนในข้อ 2
4.เมื่อทอมสันเปลี่ยนชนิดของโลหะที่นำ มาทำเป็นแคโทดแล้วใช้แก๊สชนิดเดียวกัน ปรากฏว่าผลการทดลองเหมือนในข้อ 2
ผลการทดลองในข้อ 3 และ 4 แสดงให้เห็นว่าไม่ว่าจะบรรจุแก๊สชนิดใดหรือใช้โลหะชนิดใดก็ตามมาทำเป็นแคโทด จะให้อนุภาคเหมือนกัน ทอมสันจึงได้ทดลองต่อไปอีกว่าอนุภาคลบเหล่านี้เป็นอนุภาคชนิดเดียวกันหรือไม่ โดยทำการทดลองหาค่าประจุต่อมวลของอนุภาคลบ โดยเอาสนามไฟฟ้าภายนอกและสนามแม่เหล็กมาตั้งฉากกัน แล้วนำไปล่อลำอนุภาคลบในหลอดรังสีแคโทด พบว่าอนุภาคลบไม่เบี่ยงเบนไปจากแนวเดิม(เกิดจุดสว่างตรงจุดกึ่งกลางของฉากเรืองแสง ที่จุด B) ตรงจุดนี้ทอมสันจึงสรุปว่าสสารทุกชนิดประกอบด้วยอนุภาคที่เป็นลบและเรียกอนุภาคนี้ว่า อิเล็กตรอน
แหล่งที่มา
ทบวงมหาวิทยาลัย. (2541). เคมี เล่ม 1 . กรุงเทพฯ: อักษรเจริญทัศน์.
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี. (2548). หนังสือเรียนเคมี พื้นฐานและเพิ่มเติม เล่ม 1 ชั้นมัธยมศึกษาปีที่ 4. กรุงเทพฯ: โรงพิมพ์คุรุสภาลาดพร้าว.
แนวคิดในการพัฒนาแบบจําลองอะตอม . สืบค้นเมื่อ 27 มิถุนายน 2560, จาก https://sites.google.com/site/khemikhrupanpan/bth-thi1/william-crookes. จาก http://komsan1022.blogspot.com/
อะตอม . สืบค้นเมื่อ 27 มิถุนายน 2560, จาก https://sites.google.com/site/phiraporn05/khorngsrang-xatxm-1
กลับไปที่เนื้อหา



