สมดุลเคมี
สมดุลเคมี (Chemical equilibrium) คือสภาวะที่ความเข้มข้นของสารตั้งต้นและสารผลิตภัณฑ์ไม่เปลี่ยนแปลงอีกแม้เวลาผ่านไป เราจะเรียกว่าปฏิกิริยาเคมีนั้นอยู่ในสมดุล (equilibrium)

ภาพการเข้าสู่สมดุลเคมีของสารอินทรีย์ Methyl tert-butyl ether (MTBE) ที่สกัดด้วยสารละลายโซเดียมไบคาร์บอร์เนตในน้ำ
ที่มา : https://th.wikipedia.org/wiki/สมดุลเคมี
กระบวนการเปลี่ยนแปลงทางวิทยาศาสตร์มี 3 รูปแบบ คือ การเปลี่ยนสถานะ การละลาย และการเกิดปฏิกิริยาเคมี จำแนกเป็น 2 ลักษณะคือ
- การเปลี่ยนแปลงที่เกิดขึ้นทางเดียวไม่ย้อนกลับ (Inreversible reaction) หมายถึงเมื่อสิ่งหนึ่งเปลี่ยนแปลงไปเป็นอีกสิ่งหนึ่งแล้ว สิ่งที่เกิดขึ้นจากการเปลี่ยนแปลงนี้จะไม่สามารถเปลี่ยนกลับมาสู่ภาวะเดิมได้โดยทันที เช่น การเผาไหม้ของสิ่งต่าง ๆ เราไม่สามารถทำให้สิ่งที่เกิดจากการเผาไหม้ เปลี่ยนกลับไปเป็นสารเดิมเหมือนก่อนการเผาไหม้ได้อีก การเปลี่ยนแปลงลักษณะนี้ไม่มีภาวะสมดุล เช่น ปฏิกิริยาการเผาไหม้ดังสมการ
CH4(g) + O2(g) CO2(g) + H2O(g)
- การเปลี่ยนแปลงที่ผันกลับได้หรือย้อนกลับได้ (Reversible reaction) มีลักษณะที่สำคัญคือเมื่อสิ่งหนึ่งเปลี่ยนแปลงไปเป็นสิ่งใหม่แล้ว สิ่งใหม่ที่เกิดขึ้นก็สามารถเปลี่ยนกลับมาเป็นสิ่งเดิมได้ทันที การเปลี่ยนแปลงลักษณะนี้จะเกิดภาวะสมดุลขึ้นได้ เช่น การผลิต ก๊าซแอมโมเนีย (NH3) จากปฏิกิริยาระหว่างก๊าซไฮโดรเจน (H2) กับก๊าซไนโตรเจน (N2) ดังสมการ
3 H2(g) + N2(g) ↔ 2NH3(g)
ในการเกิดปฏิกิริยานี้ ก๊าซ H2 และ N2 เป็นสารตั้งต้น ทำปฏิกิริยากันกลายเป็นก๊าซ NH3 และในทันทีที่เกิดก๊าซ NH3 ก๊าซ NH3 ที่เกิดขึ้นจะสลายตัวกลับไปเป็นก๊าซ H2 และ N2 อย่างเดิม ฉะนั้นในเวลาเดียวกันจึงมีการเปลี่ยนแปลงเกิดขึ้น 2 กระบวนการพร้อมกัน ได้แก่
2.1 ก๊าซ H2 กับ N2 ทำปฏิกิริยากันกลายเป็นก๊าซ NH3 ดังสมการ
3 H2(g) + N2(g) → 2NH3(g)
กระบวนการนี้เกิดขึ้นก่อน เรียกว่าการเปลี่ยนแปลงไปข้างหน้า (forward change หรือ forward reaction)
2.2 ก๊าซ NH3 บางส่วนสลายตัวกลับมาเป็นก๊าซ H2 กับ N2 ตามเดิม ดังสมการ
2NH3(g) → 3H2(g) + N2(g)
กระบวนการนี้เกิดขึ้นทีหลัง เรียกว่าการเปลี่ยนแปลงย้อนกลับ (reverse change หรือ reverse reaction) เมื่อนำการเปลี่ยนแปลงทั้ง 2 มาเขียนไว้ในสมการเดียวกัน รูปของสมการจะเป็นดังนี้
2NH3(g) ⇌ 3H2(g) + N2(g)
ภาวะสมดุล หมายถึง ภาวะที่ระบบมีสมบัติคงที่ หรือภาวะที่สารตั้งต้นและสารผลิตภัณฑ์ทุกชนิดมีปริมาณหรือความเข้มข้นคงที่ หรือภาวะที่อัตราการเปลี่ยนแปลงไปข้างหน้าเท่ากับอัตราการเปลี่ยนแปลงย้อนกลับ
สมบัติของระบบ ณ ภาวะสมดุล
-
ต้องเป็นปฏิกิริยาที่ผันกลับได้ โดย ต้องเกิดในระบบปิด
-
มีปฏิกิริยาไปข้างหน้าและย้อนกลับเกิดขึ้นตลอดเวลา โดยจำนวนโมลของสารตั้งต้นและผลิตภัณฑ์คงที่แต่อาจเท่ากันหรือไม่เท่ากันก็ได้ และ อัตราการเกิดปฏิกิริยาไปข้างหน้าเท่ากับปฏิริยาย้อนกลับ
-
สมบัติของระบบคงที่ (จำนวนโมลคงที่ สีของสารคงที่ ความดันคงที่ และอุณหภูมิคงที่)
ภาวะสมดุลระหว่างสถานะ สารต่างๆสามารถเปลี่ยนสถานะได้ โดยมีการเปลี่ยนแปลงพลังงานควบคู่ไปด้วย ดังแผนภาพนี้
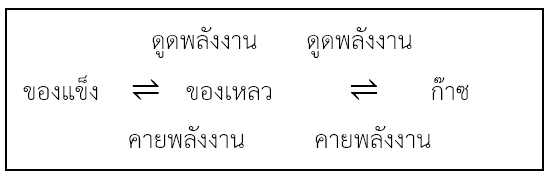
ที่ภาวะสมดุลของปฏิกิริยาเคมีระบบยังมิได้หยุดนิ่ง ยังมีทั้งการเกิดปฏิกิริยาไปข้างหน้า และเกิดปฏิกิริยาย้อนกลับตลอดเวลาโดยเกิดในอัตราที่เท่ากัน เรียกภาวะสมดุลนี้ว่า ภาวะสมดุลไดนามิก
ภาวะสมดุลในสารละลายอิ่มตัว เมื่อให้ตัวถูกละลาย ละลายในตัวทำละลาย ตัวถูกละลายก็จะละลายได้เร็วในตอนแรกแล้วละลายได้ช้าลงและเมื่อเกิดสารละลายอิ่มตัว เราจะพบว่าตัวถูกละลายไม่ละลายต่อไปอีก ไม่ว่าจะคนสารละลายเป็นเวลานานเท่าใดถ้าอุณหภูมิคงที่ เมื่อตั้งสารละลายอิ่มตัวไว้จะเกิดผลึกขึ้นและปริมาณของผลึกจะเพิ่มขึ้นเรื่อยๆจนในที่สุดผลึกคงที่ เรายังดูเหมือนว่าไม่เกิดผลึกอีก แต่ในระบบผลึกยังคงเกิดขึ้นเรื่อยๆแล้วก็ละลายในสารละลายอีกด้วย
สมดุลในปฏิกิริยาเคมี คือ ปฏิกิริยาเคมีที่เกิดภาวะสมดุลจะต้องเป็นปฏิกิริยาผันกลับได้ และ สมบัติของระบบต้องคงที่ การศึกษาภาวะสมดุลของปฏิกิริยาเคมี ตรวจสอบดังนี้
-
ทดสอบปฏิกิริยาไปข้างหน้า (สารตั้งต้นทำปฏิกิริยากันแล้วเกิดเป็นสารผลิตภัณฑ์หรือไม่)
-
ทดสอบปฏิกิริยาย้อนกลับ (นำสารผลิตภัณฑ์มาทำปฏิกิริยากันแล้วกลับไปเป็นสารตั้งต้นหรือไม่)
-
สังเกตสมบัติของระบบว่าคงที่หรือไม่ (อาจสังเกตสีว่าคงที่หรือไม่)
การเปลี่ยนแปลงที่ก่อให้เกิดสมดุลเคมีต้องเป็นการเปลี่ยนแปลงที่ผันกลับได้ ซึ่งแบ่งเป็น 3 ประเภท ดังนี้
1.) การเปลี่ยนสถานะ
เช่น การกลายเป็นไอของน้ำในภาชนะปิด น้ำเปลี่ยนสถานะจากของเหลวเป็นแก๊ส
H2O(l) ⇌ H2O(g)
หรือการระเหิดของไอโอดีนในภาชนะปิด ซึ่งเปลี่ยนสถานะไอโอดีนจากของแข็งเป็นแก๊ส
I2(s) ⇌ I2 (g)
ดังนั้น ในระบบอาจมีการเปลี่ยนสถานะจากของแข็งเป็นของเหลว หรือจากของเหลวเป็นแก๊ส หรือจากแก๊สเป็นของแข็งอย่างใดอย่างหนึ่ง ดังนั้นการเปลี่ยนสถานะที่จะก่อให้เกิดสมดุลเคมีได้ต้องเกิดในระบบปิดเท่านั้น
2) การเกิดสารละลาย
การเกิดสารละลายที่จะก่อให้เกิดสมดุลเคมี เช่น การละลายของเกลือ NaCl ในน้ำได้สารละลาย แต่เมื่อให้ความร้อนจะเกิดเป็นสารละลายอิ่มตัว เมื่ออุณหภูมิลดลงจะเกิดการตกผลึกของเกลือ NaCl กลับมา การเกิดสารละลายลักษณะนี้จึงก่อให้เกิดการเปลี่ยนแปลงที่ผันกลับได้ การละลายของเกลือแกงแสดงดังสมการข้างล่าง(จะต้องละลายจนอิ่มตัวจึงจะเกิดสมดุล)
NaCl (s) + H2O ⇌ Na+(aq) + Cl- (aq)
3) การเกิดปฏิกิริยาเคมี
การเกิดปฏิกิริยาบางปฏิกิริยาสามารถผันกลับได้ และก่อให้เกิดสมดุลเคมี เช่น การละลายของก๊าซ CO2 ในน้ำ อาจจะเกิดการเปลี่ยนแปลงในลักษณะการแพร่ของแก๊ส CO2 ในน้ำ หรืออาจเกิดปฏิกิริยาเคมีกับน้ำได้กรดคาร์บอนิก และกรดคาร์บอนิกสามารถสลายตัวกลับมาเป็นแก๊ส CO2 และ H2O เหมือนเดิม
CO2 (g) + H2O (l) ⇌ H2CO3
แหล่งที่มา
บัญชา แสนทวี และคณะ .(2551). หนังสือเรียนรายวิชาเคมีเพิ่มเติมชั้นมัธยมศึกษาปีที่ 4 - 6 หลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551. กรุงเทพฯ : สำนักงานพิมพ์วัฒนาพานิช.
พงศธร นันทธเนศ และคณะ .(2556). หนังสือเสริมสร้างศักยภาพและทักษะ เคมี เล่ม 3 ชั้นมัธยมศึกษาปีที่ 4 - 6. กรุงเทพฯ : บริษัทไทยร่มเกล้า จำกัด.
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี. (2553). หนังสือเรียนสาระการเรียนรู้พื้นฐานและเพิ่มเติม เคมี เล่ม 3 กลุ่มสาระการเรียนรู้วิทยาศาสตร์ ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551. กรุงเทพฯ: โรงพิมพ์คุรุสภาลาดพร้าว
กลับไปที่เนื้อหา
ใน พ.ศ. 2427 อ็องรี หลุยส์ เลอ ชาเตอลิเยร์ (Le Chatelier, Henry-louis) ได้ให้ข้อมูลสรุปการศึกษาการค้นคว้าเกี่ยวกับการเปลี่ยนแปลงสภาสมดุลของปฏิกิริยาต่างๆไว้ดังนี้ “เมื่อระบบที่อยู่ในภาวะสมดุลถูกรบกวนโดยการเปลี่ยนแปลงปัจจัยที่มีผลต่อภาวะสมดุลขอระบบ ระบบจะเกิดการเปลี่ยนแปลงไปในทิศทางที่จะลดผลของการรบกวนนั้น เพื่อให้ระบบเข้าสู่ภาวะสมดุลอีกครั้ง”
โดยระบบที่อยู่ในภาวะสมดุลมีสมบัติต่างๆของระบบคงที่ เช่น ความเข้มข้นของสารตั้งต้นและสารผลิตภัณฑ์คงที่ ความดันของระบบคงที่ อัตราการเกิดปฏิกิริยาไปข้างหน้าเท่ากับอัตราการเกิดปฏิกิริยาย้อนกลับ เป็นต้น การรบกวนภาวะสมดุลของระบบโดยการเปลี่ยนแปลงสภาวะของสารในปฏิกิริยา อาจทำให้ค่าคงที่ของสมดุลและตำแหน่งของภาวะสมดุลเปลี่ยนไป หรืออาจทำให้ระบบเข้าสู่ภาวะสมดุลได้เร็วขึ้นหรือช้าลง

ภาพอ็องรี หลุยส์ เลอ ชาเตอลิเยร์
ที่มา https://commons.wikimedia.org/wiki/File:Lechatelier.jpg ,
การเปลี่ยนแปลงความเข้มข้นของสาร
การเพิ่มความเข้มข้นของสาร เป็นการเพิ่มจำนวนโมเลกุลของสารที่เข้าทำปฏิกิริยาให้มีโอกาสชนกันมากขึ้น ทำให้อัตราการเกิดปฏิกิริยาเพิ่มขึ้น แต่การลดความเข้มข้นของสารเป็นการลดจำนวนโมเลกุลของสารที่เข้าทำปฏิกิริยา ทำให้อัตราการเกิดปฏิกิริยาลดลง
การเปลี่ยนแปลงความเข้มข้นของสารในปฏิกิริยาเคมี โดยทั่วไปมีผลต่อภาวะสมดุลของระบบดังนี้
-
การเพิ่มความเข้มข้นของสารตั้งต้นสารใดสารหนึ่ง สมดุลจะเลื่อนไปทางขวา และเมื่อเพิ่มความเข้มข้นของสารผลิตภัณฑ์สารใดสารหนึ่ง สมดุลจะเลื่อนไปทางซ้าย
-
การลดความเข้มข้นของสารตั้งต้นสารใดสารหนึ่ง สมดุลจะเลื่อนไปทางซ้าย และเมื่อลดความเข้มข้นของสารผลิตภัณฑ์สารใดสารหนึ่ง สมดุลจะเลื่อนไปทางขวา
-
สารที่มีสถานะเป็นของแข็ง (s) หรือของเหลวบริสุทธิ์ (l) จะไม่มีผลต่อภาวะสมดุลของระบบ เนื่องจากมีค่าความเข้มข้นคงที่
โดยเมื่อเปลี่ยนความเข้มข้นของสารในระบบ ภาวะสมดุลของระบบจะเปลี่ยนแปลงด้วย แต่ไม่มีผลต่อค่าคงที่สมดุลของระบบ คือ ค่าคงที่สมดุลของระบบจะมีค่าคงที่ถึงแม้ว่าจะเพิ่มหรือลดความเข้มข้นของสารตั้งต้นหรือผลิตภัณฑ์ก็ตาม
การเปลี่ยนแปลงความดันของระบบ
การเปลี่ยนแปลงความดันหรือปริมาตรจะมีผลต่อภาวะสมดุลก็ต่อเมื่อ
-
ต้องเป็นภาวะสมดุลของระบบที่มีสารอย่างน้อยหนึ่งชนิดเป็นแก๊ส ถ้าเป็นระบบที่มีสารตั้งต้นและสารผลิตภัณฑ์เป็นของแข็งหรือของเหลว การเปลี่ยนแปลงความดันจะไม่มีผลต่อภาวะสมดุลของระบบ
-
จำนวนโมลของสารตั้งต้นที่เป็นแก๊ส ต้องไม่เท่ากับจำนวนโมลของสารผลิตภัณฑ์ที่เป็นแก๊ส
โดยการเปลี่ยนแปลงความดันกับภาวะสมดุลของระบบที่มีแก๊สเกี่ยวข้องและจำนวนโมลของแก๊สตั้งต้น และจำนวนโมลของแก๊สผลิตภัณฑ์ต้องไม่เท่ากัน การเปลี่ยนแปลงความดันจะมีผลในการทำให้ภาวะสมดุลเปลี่ยนไป คือ
- การเพิ่มความดัน เมื่อเพิ่มความดันให้แก่ระบบ (ลดปริมาตรของระบบ) ระบบจะปรับตัวไปในทิศทางลดความดัน โดยการลดจำนวนโมลหรือโมเลกุลของระบบลง เพราะความดันเป็นสัดส่วนโดยตรงกับจำนวนโมลหรือโมเลกุล ดังนั้นการเพิ่มความดันจะทำให้ปฏิกิริยาเกิดไปทางด้านที่มีจำนวนโมลหรือโมเลกุลของแก๊สที่มีจำนวนโมลน้อยกว่าได้ดีขึ้น ที่ภาวะสมดุลใหม่ความเข้มข้นของสารจะต่างจากภาวะสมดุลเดิม
- การลดความดัน เมื่อลดความดันให้แก่ระบบ (เพิ่มปริมาตรของระบบ) ระบบจะปรับตัวไปในทิศทางเพิ่มความดัน โดยการเพิ่มจำนวนโมลหรือโมเลกุลของระบบลง เพราะความดันเป็นสัดส่วนโดยตรงกับจำนวนโมลหรือโมเลกุล ดังนั้นการลดความดันจะทำให้ปฏิกิริยาเกิดไปทางด้านที่มีจำนวนโมลหรือโมเลกุลของแก๊สที่มีจำนวนโมลมากกว่าได้ดีขึ้น ที่ภาวะสมดุลใหม่ความเข้มข้นของสารจะต่างจากภาวะสมดุลเดิม
กรณีการเปลี่ยนความดันกับภาวะสมดุลของระบบที่มีแก๊สเข้ามาเกี่ยวข้อง แต่มีจำนวนโมลของสารตั้งต้นที่เป็นแก๊สเท่ากับจำนวนโมลของสารผลิตภัณฑ์ที่เป็นแก๊ส การเพิ่มหรือลดความดันจะไม่มีผลต่อภาวะสมดุลของระบบ เพราะจำนวนโมลของสารตั้งต้นที่เป็นแก๊สเท่ากับจำนวนโมลของสารผลิตภัณฑ์ที่เป็นแก๊สเท่ากัน ดังนั้นไม่ว่าจะเกิดปฏิกิริยาไปข้างหน้าหรือย้อนกลับจำนวนโมลของสารที่มีสถานะแก๊สภายในระบบก็ไม่เปลี่ยนแปลง เมื่อเปลี่ยนความดันอัตราการเกิดปฏิกิริยาไปข้างหน้าและย้อนกลับยังคงเท่ากันตลอดเวลา
การเปลี่ยนแปลงอุณหภูมิของระบบ
กรณีที่ 1 การเปลี่ยนแปลงอุณหภูมิกับภาวะสมดุลของปฏิกิริยาดูดความร้อน คือ ΔE มีค่าเป็นบวกในปฏิกิริยาดูดความร้อน เมื่อมีการเปลี่ยนแปลงอุณหภูมิจะทำให้ภาวะสมดุลเปลี่ยนไป ดังนี้
-
การเพิ่มอุณหภูมิ เมื่อเพิ่มอุณหภูมิของระบบ ระบบจะต้องปรับตัวไปในทิศทางลดอุณหภูมิของระบบลง โดยระบบจะดูดความร้อนไปใช้ในการเกิดปฏิกิริยามากขึ้น ดังนั้นเมื่อเพิ่มอุณหภูมิระบบปฏิกิริยาจะเกิดไปทางด้านดูดความร้อนมากขึ้น หรือเกิดปฏิกิริยาไปข้างหน้ามากขึ้น
-
การลดอุณหภูมิ เมื่อลดอุณหภูมิของระบบลดลง ระบบจะต้องปรับตัวไปในทิศทางเพิ่มอุณหภูมิของระบบลง ดังนั้นเมื่อลดอุณหภูมิระบบปฏิกิริยาจะเกิดไปทางด้านคายความร้อนออกมา หรือเกิดปฏิกิริยาย้อนกลับเพื่อเพิ่มอุณหภูมิของระบบขึ้น
กรณีที่ 2 การเปลี่ยนแปลงอุณหภูมิกับภาวะสมดุลของปฏิกิริยาคายความร้อน คือ ΔE มีค่าเป็นลบในปฏิกิริยาคายความร้อน เมื่อมีการเปลี่ยนแปลงอุณหภูมิจะทำให้ภาวะสมดุลเปลี่ยนไป ดังนี้
-
การเพิ่มอุณหภูมิ เมื่อเพิ่มอุณหภูมิของระบบลดลง ระบบจะต้องปรับตัวไปในทิศทางลดอุณหภูมิของระบบลง ดังนั้นเมื่อเพิ่มอุณหภูมิระบบปฏิกิริยาจะเกิดไปทางด้านดูดความร้อนหรือเกิดปฏิกิริยาย้อนกลับได้ดีขึ้น เมื่อความร้อนถูกใช้ไปมากขึ้นก็จะทำให้อุณหภูมิลดต่ำลง
-
การลดอุณหภูมิ เมื่อลดอุณหภูมิของระบบ ระบบจะต้องปรับตัวไปในทิศทางเพิ่มอุณหภูมิของระบบลง ดังนั้นเมื่อลดอุณหภูมิระบบปฏิกิริยาจะเกิดไปทางด้านคายความร้อนหรือเกิดปฏิกิริยาไปข้างหน้าได้ดีขึ้น เมื่อปฏิกิริยาคายความร้อนออกมาก็จะทำให้อุณหภูมิสูงขึ้น
โดย ผลของการเปลี่ยนแปลงอุณหภูมินั้น ถ้าเป็นปฏิกิริยาคายความร้อน การลดอุณหภูมิทำให้ผลิตภัณฑ์มากขึ้นและค่าคงที่สมดุลสูงขึ้น แต่ถ้าเป็นปฏิกิริยาดูดความร้อน การลดอุณหภูมิทำให้ได้ผลิตภัณฑ์น้อยลงและค่าคงที่สมดุลลดลง ส่วนการเพิ่มอุณหภูมินั้นจะทำให้ถ้าเป็นปฏิกิริยาคายความร้อน การเพิ่มอุณหภูมิทำให้ผลิตภัณฑ์น้อยลงและค่าคงที่สมดุลลดลง แต่ถ้าเป็นปฏิกิริยาดูดความร้อน การเพิ่มอุณหภูมิทำให้ได้ผลิตภัณฑ์มากขึ้นและค่าคงที่สมดุลเพิ่มขึ้น
แหล่งที่มา
บัญชา แสนทวี และคณะ .(2551). หนังสือเรียนรายวิชาเคมีเพิ่มเติมชั้นมัธยมศึกษาปีที่ 4 - 6 หลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551. กรุงเทพฯ : สำนักงานพิมพ์วัฒนาพานิช.
พงศธร นันทธเนศ และคณะ .(2556). หนังสือเสริมสร้างศักยภาพและทักษะ เคมี เล่ม 3 ชั้นมัธยมศึกษาปีที่ 4 - 6. กรุงเทพฯ : บริษัทไทยร่มเกล้า จำกัด.
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี. (2553). หนังสือเรียนสาระการเรียนรู้พื้นฐานและเพิ่มเติม เคมี เล่ม 3 กลุ่มสาระการเรียนรู้วิทยาศาสตร์ ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551. กรุงเทพฯ: โรงพิมพ์คุรุสภาลาดพร้าว
กลับไปที่เนื้อหา
กระบวนการหายใจและการแลกเปลี่ยนแก๊สในระบบหมุนเวียนเลือด
การดำรงชีวิตของมนุษย์จะเกี่ยวข้องกับกระบวนการและปฏิกิริยาต่างๆภายในร่างกาย ซึ่งเกิดขึ้นในลักษณะของสมดุลไดนามิก เช่น กระบวนการหายใจและแลกเปลี่ยนแก๊สในระบบหมุนเวียนเลือด ในภาวะปกติขณะที่ร่างกายพักผ่อน กระบวนการหายใจเป็นกระบวนการที่เฮโมโกลบินรับแก๊สออกซิเจนที่แพร่ผ่านเนื้อเยื่อของถุงลมเข้าสู่เส้นเลือดฝอย แล้วรวมกับเฮโมโกลบินในเม็ดเลือดแดงได้ออกซีเฮโมโกลบิน ขณะหายใจเข้า ความดันของ O2 ในถุงลมปอดสูงกว่าในเส้นเลือดฝอย ปฏิกิริยาจึงดำเนินไปข้างหน้า จึงเกิดออกซีเฮโมโกลบินมาก ซึ่งจะไหลเวียนไปสู่เซลล์ต่างๆ ของร่างกายเพื่อนำ O2 ไปสันดาปกับสารอาหารในเซลล์ ผลจากการสันดาปอาหารจะได้แก๊ส CO2 กับน้ำ และพลังงาน
ขณะหายใจเข้า จะผ่านหลอดลมฝอยเข้าสู่ถุงลมปอด ความดันของ ในถุงลมปอดจะสูงกว่าความดันในเส้นเลือดฝอย จากถุงลมปอดจึงแพร่ผ่านเนื้อเยื่อของถุงลมปอดเข้าสู่เส้นเลือดฝอยและรวมตัวกับเฮโมโกลบินที่เม็ดเลือดแดงกลายเป็นออกซีเฮโมโกลบิน ปฏิกิริยาจะดำเนินไปข้างหน้า เมื่อเลือดไหลเวียนไปยังเนื้อเยื่อต่าง ๆ ของร่างกายซึ่งจำเป็นต้องใช้ เพื่อทำกิจกรรมต่าง ๆ ที่เป็นผลจากเมแทบอลิซึม ในเลือดจึงถูกปล่อยออกมา ปฏิกิริยาจะเกิดในทิศทางย้อนกลับเพื่อเพิ่มปริมาณ เนื่องจากกระบวนการทั้งสองนี้ดำเนินไปอย่างต่อเนื่องรวมทั้งมีอัตราการเกิดปฏิกิริยาไปข้างหน้าและปฏิกิริยาย้อนกลับเท่ากัน จึงทำให้มีภาวะสมดุล
ในกระบวนการหายใจ นอกจากจะมีการปรับสมดุลของ แล้ว ให้นักเรียนพิจารณาสมการแสดงปฏิกิริยาที่เกิดขึ้นในกระบวนการเมแทบอลิซึมของกลูโคสซึ่งใช้ออกซิเจนต่อไปนี้
C6H12O6 + O2 CO2 + H2O
จากสมการทำให้ทราบว่าในการเผาผลาญกลูโคส 1 โมเลกุล จะต้องใช้ จำนวนมากและทำให้เกิด มากด้วยเช่นกันเมื่อ ที่เนื้อเยื่อมีปริมาณสูง จะแพร่เข้าสู่เลือดในหลอดเลือดฝอยเพื่อส่งผ่านไปยังปอด ซึ่ง จะทำปฏิกิริยากับน้ำเกิดเป็นกรดคาร์บอนิก และแตกตัวอยู่ในรูปของไฮโดรเจนคาร์บอเนตไอออน กับไฮโดรเจนไอออน เมื่อไฮโดรเจนคาร์บอเนตไอออนถูกส่งถึงหลอดฝอยรองถุงลมปอด ซึ่งภายในถุงลมปอดมีความดันของ น้อยปฏิกิริยาจะเกิดย้อนกลับเพื่อเพิ่มความดัน โดย ในหลอดเลือดฝอยจะแพร่เข้าสู่ถุงลมปอดและถูกขับออกจากปอดในขณะที่เราหายใจออก ระบบการส่ง และ ของร่างกาย จากการศึกษาพบว่าในเลือดของคนที่อาศัยอยู่ในพื้นที่สูงกว่าระดับน้ำทะเลมาก ๆ จะมีความเข้มข้นของเฮโมโกลบินในเม็ดเลือดแดงสูง แสดงว่าภาวะแวดล้อมที่แตกต่างกันเป็นปัจจัยที่มีผลต่อการทำงานของระบบต่าง ๆ ภายในร่างกาย ดังนั้นผู้ที่ต้องเดินทางไปในพื้นที่สูงกว่าระดับน้ำทะเลมาก ๆ อาจเกิดอาการที่เรียกว่า ไฮพอกเซีย (hypoxia) ซึ่งเกิดจากการที่มีออกซิเจนไปเลี้ยงเนื้อเยื่อของร่างกายไม่เพียงพอ ทำให้มีอาการปวดศีรษะ คลื่นไส้ และอ่อนเพลีย ในรายที่เป็นรุนแรงอาจถึงตายได้เนื่องจากความดันของออกซิเจนที่ระดับความสูงจากระดับน้ำทะเลมากๆ มีค่าต่ำกว่าความดันของออกซิเจนในบรรยากาศมีค่าประมาณ 0.14 บรรยากาศ ส่วนความดันย่อยของออกซิเจนในบรรยากาศที่ระดับน้ำทะเลมีค่าประมาณ 0.2 บรรยากาศ ดังนั้นการอยู่ในที่ระดับความสูงมากๆ จึงมีปริมาณของ O2 ในอากาศลดลง ตามหลักของเลอชาเตอลิเอ เมื่อความเข้มข้นของสารตั้งต้นในที่นี้คือออกซิเจนลดลง ปฏิกิริยาย้อนกลับจะเกิดมากขึ้น ทำให้ปริมาณของออกซีเฮโมโกลบินลดลง เป็นผลให้การขนส่ง O2 ไปเลี้ยงเนื้อเยื่อส่วนต่างๆได้น้อยลง จึงทำให้เกิดอาการไฮพอกเซีย อย่างไรก็ตามถ้าอยู่ในบริเวณนั้นนานๆ ร่างกายสามารถปรับตัวโดยสร้าง Hb ในเลือดให้เพิ่มมากขึ้นจนมีผลให้เฮโมโกลบินสามารถจับกับ O2เกิดเป็นออกซีเฮโมโกลบินได้อย่างเพียงพอ ด้วยเหตุนี้คนที่อยู่ในบริเวณที่มีความสูงมากๆ จึงมีระดับความเข้มข้นของเฮโมโกลบินในเลือดสูงกว่าของคนที่อยู่ที่ระดับน้ำทะเลปกติ เนื่องจากกระบวนการทั้งสองเกิดขึ้นอย่างต่อเนื่องและมีอัตราการเกิดปฏิกิริยาไปข้างหน้าและปฏิกิริยาย้อนกลับเท่ากัน ในที่สุดระบบก็จะปรับตัวเข้าสู่ภาวะสมดุล
ภาวะสมดุลของแคลเซียมในร่างกาย
ในร่างกายประกอบด้วยกระดูกซึ่งทำหน้าที่เป็นโครงสร้างสำคัญของร่างกาย ทำให้คนรูปร่างแตกต่างกันไปตามลักษณะโครงกระดูกที่มีทั้งกระดูกแกนกลางและกระดูกรยางค์ ซึ่งมีธาตุแคลเซียมเป็นองค์ประกอบสำคัญประมาณร้อยละ 98-99 ที่เหลืออีกร้อยละ 1-2 จะอยู่ในเนื้อเยื่อและกระแสเลือด โดยการรักษาภาวะสมดุลของธาตุแคลเซียมที่มีอยู่ในกระแสเลือดกับปริมาณธาตุแคลเซียมในกระดูกโดยมีวิตามินดีและฮอร์โมนจากต่อมพาราไทรอยด์ช่วยควบคุม ทำให้การทำงานของระบบต่างๆของร่างกายเป็นไปตามปกติ
ภาวะสมดุลกับการเปลี่ยนแปลงเพศของสัตว์บางชนิด
สัตว์บางชนิดมีอัตราส่วนระหว่างเพศผู้กับเพศเมียเท่ากัน ตามธรรมชาติสัตว์บางประเภทจะมีการเปลี่ยนแปลงเพศเพื่อตอบสนองต่อสิ่งแวดล้อมภายนอกที่มากระทบ เพื่อเป็นการปรับภาวะสมดุล เช่น ปลาแอตแลนติก ซิลเวอร์ไซด์ (Atlantic zilverside fish) เปลี่ยนเพศตัวเองเมื่ออุณหภูมิของน้ำและสิ่งแวดล้อมสูงขึ้น สัตว์อื่นๆเช่น กบแอฟริกัน (African Reed frog) เพศเมียและปลาแอนเทเรียส
สคอมิพินนิส (Anthias squamipinnis fish) จะเปลี่ยนเพศเมื่อปลาเพศผู้มีปริมาณลดลง การเปลี่ยนแปลงเพศของประชากรปลามีผลต่อภาวะสมดุล และมีการปรับภาวะสมดุลในธรรมชาติ ดังนี้
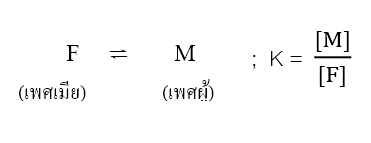
ภาวะสมดุลของวัฏจักรคาร์บอน
ธาตุคาร์บอนเป็นองค์ประกอบของสารจำนวนมากทั้งในสิ่งมีชีวิตและไม่มีชีวิต พบได้ในเชื้อเพลิงซึ่งเป็นสารประกอบไฮโดรคาร์บอน ในหินปูน เปลือกหอย เปลือกไข่ และปะการัง ซึ่งเป็นสารประกอบประเภทคาร์บอเนต การหมุนเวียนของธาตุคาร์บอนระหว่างบรรยากาศกับแหล่งน้ำจะอยู่ในรูปของสารประกอบ CO2 ในขณะที่ CO2 จากกระบวนการหายใจ เผาไหม้ และการเน่าเปื่อยเข้าสู่บรรยากาศนั้น บางส่วนละลายอยู่ในแหล่งน้ำบนพื้นโลก
แหล่งที่มา
บัญชา แสนทวี และคณะ .(2551). หนังสือเรียนรายวิชาเคมีเพิ่มเติมชั้นมัธยมศึกษาปีที่ 4 - 6 หลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551. กรุงเทพฯ : สำนักงานพิมพ์วัฒนาพานิช.
พงศธร นันทธเนศ และคณะ .(2556). หนังสือเสริมสร้างศักยภาพและทักษะ เคมี เล่ม 3 ชั้นมัธยมศึกษาปีที่ 4 - 6. กรุงเทพฯ : บริษัทไทยร่มเกล้า จำกัด.
สถาบันส่งเสริมการสอนวิทยาศาสตร์และเทคโนโลยี. (2553). หนังสือเรียนสาระการเรียนรู้พื้นฐานและเพิ่มเติม เคมี เล่ม 3 กลุ่มสาระการเรียนรู้วิทยาศาสตร์ ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551. กรุงเทพฯ: โรงพิมพ์คุรุสภาลาดพร้าว
กลับไปที่เนื้อหา
-
คำที่เกี่ยวข้อง



