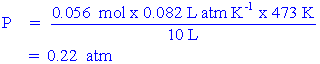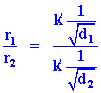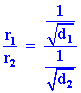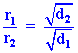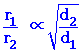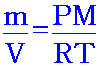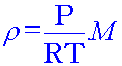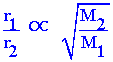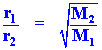กฏของแก๊สจริงและแก๊สอุดมคติ
![]()
บทเรียนที่ 1 กฎของบอยล์
![]()

โรเบิร์ต บอยล์ (Robert Boyle) ค.ศ. 1627 - 1691
มีนักวิทยาศาสตร์หลายกลุ่มพยายามศึกษาเรื่องแก๊ส โรเบิร์ต บอยล์ นักวิทยาศาสตร์ ชาวอังกฤษ ก็เป็นคนหนึ่งที่สนใจศึกษาสมบัติของแก๊สด้วย ในการศึกษาเรื่องแก๊สจะมีตัวแปรที่สำคัญอยู่ 4 ตัวแปร คือความดัน ปริมาตร อุณหภูมิ และปริมาณของแก๊ส เพราะฉะนั้นเมื่อเราต้องการสังเกตผลของตัวแปรหนึ่งซึ่งเกิดจากการเปลี่ยนแปลงของอีกตัวแปรหนึ่ง จึงต้องควบคุมตัวแปรอีกสองตัวให้คงที่ โรเบิร์ต บอยล์ก็เช่นเดียวกัน เมื่อเขาศึกษาเรื่องแก๊ส เขาจะศึกษาว่า เมื่อความดันเปลี่ยนไป ปริมาตรของแก๊สจะเปลี่ยนไปอย่างไร โดยการทำการทดลองที่อุณหภูมิเท่ากัน และ ปริมาณของแก๊สก็กำหนดให้คงที่ เขาทำการทดลองอย่างไรกัน
การทดลองของบอยล์ ก่อนที่จะได้ข้อสรุป เขาได้ใช้เครื่องมือที่มีลักษณะดังรูป

เครื่องมือนี้ สร้างโดย โรเบิร์ต ฮุค (Robert Hooke) ผู้ช่วยของเขา เครื่องมือประกอบด้วย 2 ส่วน คือถังอากาศและปั๊ม ถังอากาศเอาไว้บรรจุอากาศ ส่วนปั๊มประกอบไปด้วย ท่อทรงกระบอก ฝาสูบ ที่จับ ซึ่งส่วนนี้จะติดแน่นกับขาสามขาที่ตั้งอยู่ ระหว่างส่วนถังอากาศมีวาล์วเปิด-ปิดให้อากาศเข้าออกได้ เครื่องมือนี้ บอยล์ใช้หาความสัมพันธ์ระหว่างความดันและปริมาตรของอากาศที่อยู่ในท่อทรงกระบอกโดยการเลื่อนฝาสูบขึ้นลง ปริมาตรและความดันของอากาศภายในก็จะเปลี่ยนไปด้วย
อีกวิธีการหนึ่งที่ใช้หาความสัมพันธ์ระหว่างความดันและปริมาตรของแก๊สคือการใช้หลอดแก้วรูปตัวยูกับปรอท
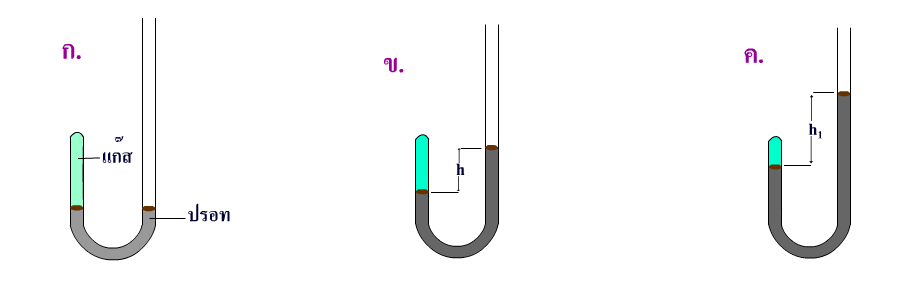
หลอดแก้วรูปตัวยู (U) มีปลายสองด้าน ด้านหนึ่งเปิด ปลายอีกด้านหนึ่งปิดสนิท กักอากาศปริมาณหนึ่งไว้ภายในหลอดโดยการเติมปรอทเข้าไปในหลอดทางด้านปลายเปิดเมื่อปรับระดับผิวปรอทในปลายสองด้านเท่ากันดังรูป ก. (เขาปรับระดับปรอทให้เท่ากันได้อย่างไรลองคิดดูซิ) แสดงว่าความดันที่กระทำต่อผิวปรอททั้งด้านปลายปิดและผิวปรอทด้านปลายเปิดเท่ากันและทำการทดลองที่ความดันบรรยากาศนั่นคือแก๊สมีความดันเท่ากับความดันบรรยากาศ (1 atm)
หลังจากนั้น เติมปรอทเข้าไปด้านปลายเปิดปริมาณหนึ่งทำให้ลำปรอทในหลอดด้านปลายเปิดสูงกว่าด้านปลายปิด ได้ความแตกต่างของลำปรอทเป็น h ดังรูป ข. พบว่า ปริมาตรแก๊สในหลอดลดลงจากเดิม และเมื่อเพิ่มปริมาณปรอทเข้าไปอีกมีความแตกต่างลำปรอทสูง h1 ปริมาตรแก๊สก็ลดลงไปอีก ดังรูป ค. การเพิ่มปริมาณปรอทเข้าไปในหลอดก็คือการเพิ่มความดันให้กับแก๊ส เพราะความสูงของปรอทด้านปลายเปิดที่สูง h หรือ h1 ย่อมมีความดันส่งผลกระทำต่อแก๊ส ทำให้ปริมาตรแก๊สในหลอดลดลงเป็นสัดส่วนโดยตรงตามความดันภายนอกที่กระทำกับแก๊ส
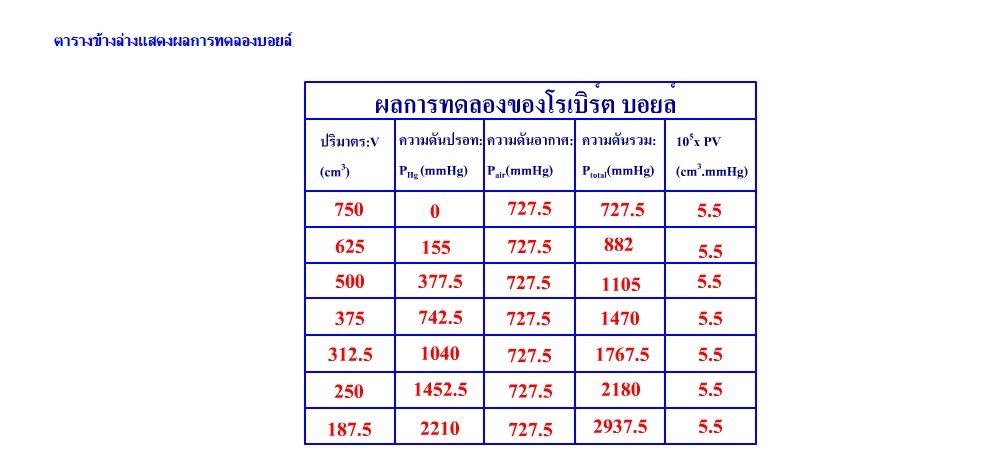
หน่วยปริมาตรเป็นลูกบาศก์เซนติเมตร(cm3) ความดันเป็นมิลลิเมตรของปรอท(mmHg) ซึ่งก็คือความแตกต่างของความสูงลำปรอท ส่วนความดันอากาศของการทดลองของบอยล์ในเวลานั้นเท่ากับ 727.5 มิลลิเมตรปรอท
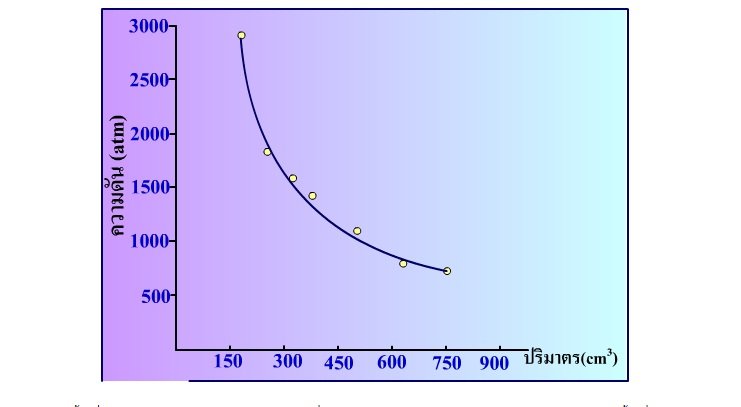
เมื่อนำข้อมูลของบอยล์ที่ได้มาเขียนกราฟ ดังรูปกราฟด้านล่าง กราฟนี้แสดงความสัมพันธ์ระหว่างความดัน(P) และปริมาตร(V)ของแก๊ส จะเห็นลักษณะกราฟเป็นเส้นโค้งไฮเปอร์โบลาร์กราฟที่ได้นี้เรียกว่าเส้นกราฟ ไอโซเทอร์ม ซึ่งหมายถึงการทำการทดลองที่อุณหภูมิคงที่ จากกราฟจะพบว่าเมื่อความดันของแก๊สเพิ่มขึ้น ปริมาตรของแก๊สจะลดลง
จากกราฟนี้เราสามารถหาพื้นที่ใต้กราฟ ณ จุดใดๆ บนเส้นกราฟ เมื่อลากไปตัดแกนความดันและแกนของปริมาตร พื้นที่ใต้กราฟจะมีค่าเท่ากันเสมอ เช่น พื้นที่ A และ B ดังรูปด้านล่าง
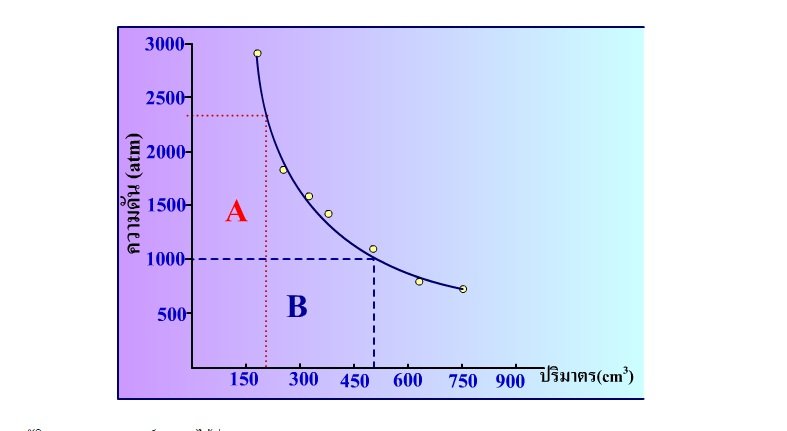
ถ้าแก๊สแสดงสมบัติตามกฏของบอยล์ เราจะได้ว่า
พื้นที่ A = พื้นที่ B
จากตารางการทดลองด้านบนเราสามารถเขียนกราฟระหว่างความดันกับปริมาตรได้อีกหลายลักษณะ ลักษณะหนึ่งคือ เมื่อให้ปริมาตรเป็นแกน y และแกน x คือ 1/P จะได้กราฟเส้นตรงตัดจุดกำเนิด ดังรูป
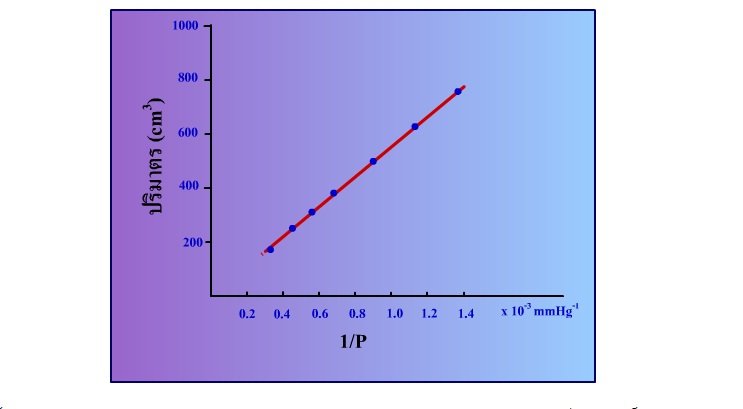
อีกแบบหนึ่งคือ เป็นความสัมพันธ์ระหว่าง ผลคูณของความดันและปริมาตร(PV) และความดัน(P) จะได้กราฟมีลักษณะเป็นเส้นตรงความชันเท่ากับศูนย์
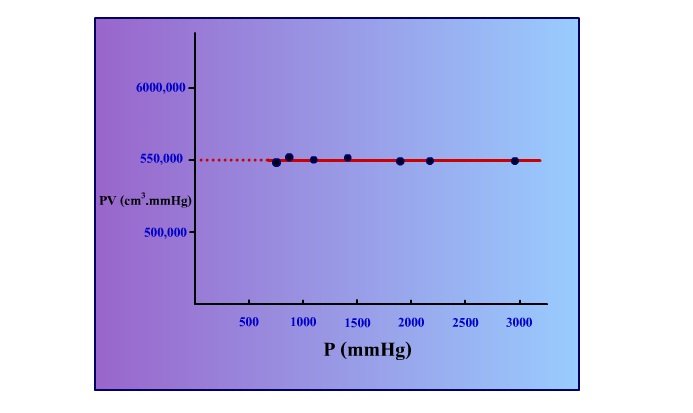
จากผลการทดลองบอยล์ เขาได้พิมพ์ผลงานที่มีชื่อว่า New Experiments Physico-Mechanical ,Touching the Spring of the Air, and Its Effectsในปี ค.ศ. 1660
กฏของบอยล์ กล่าวว่า ที่อุณหภูมิคงที่ ปริมาตรของแก๊สที่มีมวลคงที่จำนวนหนึ่งเปลี่ยนไปเป็นปฏิภาคผกผันกับความดัน
![]()
![]()
![]()
เมื่อ P และ V คือความดันและปริมาตรของแก๊สตามลำดับ
k = ค่าคงที่
ต่อมานักวิทยาศาสตร์อีกหลายท่านได้ทดลองความสัมพันธ์ของความดันแก๊สและปริมาตร ด้วยความแม่นยำมากขึ้นของแก๊สหลาย ๆ ชนิด พบว่า ผลคูณของความดันกับปริมาตรไม่ได้เป็นค่าคงที่ตามกฏของบอยล์ที่ความดันน้อยๆ แต่จะขึ้นอยู่กับความดันที่เปลี่ยนไป ที่ความดันน้อยกว่าหนึ่งบรรยากาศ ดังกราฟข้างล่าง
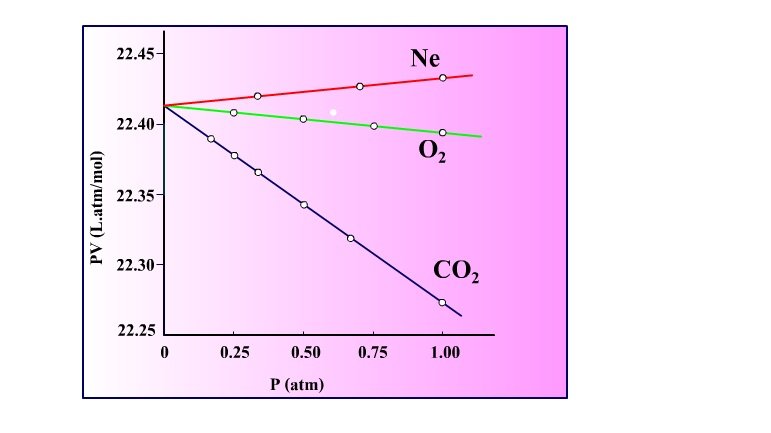
จากกราฟ แกน y คือ ผลคูณของปริมาตรและความดันแก๊สในหน่วย L.atm/mol ของแก๊สชนิดต่างๆ แกน x คือความดันของแก๊สส่วนเส้นประคือเส้นกราฟของแก๊สอุดมคติ
จากกราฟ เป็นกราฟของ แก๊สคาร์บอนไดออกไซด์(CO2) แก๊สออกซิเจน(O2) และแก๊สนีออน (Ne) แก๊สทั้ง 3 ชนิดจำนวน 1 โมล ที่ความดันแก๊สเข้าใกล้ ศูนย์ ปริมาตรของแก๊สมีค่าเท่ากับ 22.415 ลิตร เมื่อความดันเพิ่มขึ้น ผลคูณของความดันและปริมาตรของแก๊สคาร์บอนไดออกไซด์และแก๊สออกซิเจนลดลง ส่วนแก๊สนีออนจะเพิ่มขึ้น ที่ความดัน 0.5 บรรยากาศ พบว่าผลคูณของปริมาตรและความดันของแก๊สคาร์บอนไดออกไซด์ มีค่าน้อยกว่าของแก๊สออกซิเจน และของแก๊สนีออน ตามลำดับหรืออีกนัยหนึ่งก็คือที่ความดันเดียวกัน ปริมาตรของแก๊สคาร์บอนไดออกไซด์จะน้อยกว่าของแก๊สออกซิเจนและของแก๊สนีออน
เส้นกราฟที่ได้เป็นของแก๊สแต่ละชนิด มีลักษณะเป็นเส้นตรง เนื่องจากกราฟนี้เป็นความสัมพันธ์ระหว่าง PV กับ P เราสามารถเขียนสมการเส้นตรงทั่วไปของกราฟของแก๊สแต่ละชนิดได้ดังนี้
![]()
ซึ่งก็คือสมการเส้นตรงที่มีจุดตัดแกน y เท่ากับ![]() ซึ่งเป็นค่าผลคูณของความดันและปริมาตร ที่ค่าความดันของแก๊สเท่ากับศูนย์ หรือเข้าใกล้ศูนย์มากที่สุด นั่นหมายความว่า เราปล่อยให้แก๊สปริมาณหนึ่งนั้นขยายตัวได้เต็มที่ที่สุดเท่าที่แก๊สจะขยายตัวไปได้ จนถือว่าแก๊สไม่มีความดันเลยหรือความดันของแก๊สเท่ากับศูนย์ เพราะแก๊สไม่มีแรงกระทำต่อผนังเลย ณ จุดนี้ ค่าความชัน เท่ากับ
ซึ่งเป็นค่าผลคูณของความดันและปริมาตร ที่ค่าความดันของแก๊สเท่ากับศูนย์ หรือเข้าใกล้ศูนย์มากที่สุด นั่นหมายความว่า เราปล่อยให้แก๊สปริมาณหนึ่งนั้นขยายตัวได้เต็มที่ที่สุดเท่าที่แก๊สจะขยายตัวไปได้ จนถือว่าแก๊สไม่มีความดันเลยหรือความดันของแก๊สเท่ากับศูนย์ เพราะแก๊สไม่มีแรงกระทำต่อผนังเลย ณ จุดนี้ ค่าความชัน เท่ากับ![]()
จากกราฟที่ความดันเข้าใกล้ศูนย์ แก๊สทั้งสามชนิดมีค่าแอลฟา เท่ากับ 22.415 ส่วนความชันของเส้นกราฟ ของแก๊สแต่ละชนิดจะแตกต่างกันไปตามชนิดของแก๊ส จากกราฟจะพบว่า ความชันของแก๊สคาร์บอนไดออกไซด์และแก๊สออกซิเจนมีค่าเป็นลบ ส่วนแก๊สนีออนมีค่าเป็นบวก
จากกฏของบอยล์ ผลคูณของความดันกับปริมาตรของแก๊สอุดมคติเท่ากับค่าคงที่
![]()
ค่าคงที่ k ก็คือค่าแอลฟา ![]()
เราจะได้สมการ ![]() ซึ่ง
ซึ่ง ![]() เป็นค่าคงที่นั่นเอง
เป็นค่าคงที่นั่นเอง
ผลคูณความดันและปริมาตร(PV) ในกราฟเป็นค่าแสดง PV ต่อโมล ดังนั้น ถ้าจำนวนโมลของแก๊สที่ใช้ศึกษาเปลี่ยนไปสมการก็จะกลายเป็น
![]()
เมื่อ n คือจำนวนโมลของแก๊ส
จากสมการเราจึงสามารถทำนายได้ว่า ถ้าต้องการให้แก๊สจริงมีสมบัติใกล้เคียงกับแก๊สในอุดมคติมากๆ ต้อง ทำให้พจน์ บีตาคูณความดัน(![]() )น้อยกว่า พจน์แอลฟา(
)น้อยกว่า พจน์แอลฟา(![]() )มากๆ นั่นคือตัดพจน์
)มากๆ นั่นคือตัดพจน์ ![]() ทิ้งได้ หรืออีกกรณีหนึ่งคืออัตรส่วนระหว่างแอลฟากับบีตาต้องน้อยกว่าความดันมากๆ
ทิ้งได้ หรืออีกกรณีหนึ่งคืออัตรส่วนระหว่างแอลฟากับบีตาต้องน้อยกว่าความดันมากๆ
กลับไปที่เนื้อหา
บทเรียนที่ 2 กฏของชาร์ล

จ๊าค อเล็กซองดร์ เซซา ชาร์ล (Jacques Alexandre César Charles, ค.ศ.1746 - 1823)
เราทราบมาแล้วว่าสสารที่อยู่ในสถานะแก๊สมีความหนาแน่นน้อย เมื่อพิจารณาระยะห่างระหว่างโมเลกุลของแก๊สจะมีระยะทางมากกว่าของแข็งและของเหลว ตามลำดับ เมื่อได้รับความร้อนเพิ่มขึ้น แก๊สจะขยายตัวมากกว่าการขยายตัวของของเหลวและของแข็ง ตามลำดับ
![]()
ทำไม ข้างกระป๋องสเปรย์สี หรือน้ำหอมต่างๆ จึงมีคำเตือนข้อหนึ่งที่บอกว่า ห้ามนำกระป๋องสเปรย์ไปเผาไฟ หรือนำไปใกล้ความร้อน
สำหรับการทดลองเกี่ยวกับแก๊สของนักวิทยาศาสตร์ชาวฝรั่งเศส จ๊าค ชาร์ล สนใจศึกษาสมบัติของแก๊สเช่นเดียวกัน โดยการทดลองของชาร์ล ได้ศึกษาความสัมพันธ์ของปริมาตรแก๊สเมื่ออุณหภูมิเปลี่ยนแปลงไป ชาร์ลได้สนใจศึกษาเรื่องแก๊สเนื่องจากในสมัยนั้นมี การใช้อากาศร้อนทำให้บอลลูนลอยบนอากาศกำลังเป็นเรื่องที่นิยมและน่าสนใจอย่างมาก เป็นเรื่องที่นักวิทยาศาสตร์ต่างสนใจที่จะทำให้บอลลูนลอยขึ้นไปได้สูงๆ และลอยได้นานขึ้นจึงมีการพัฒนาเพื่อเพิ่มประสิทธิภาพของบอลลูนของนักวิทยาศาสตร์ต่างๆ ความสัมพันธ์ระหว่างการขยายตัวของแก๊สกับอุณหภูมิจึงเป็นเรื่องที่น่าสนใจ
รวมทั้งชาร์ลก็เช่นเดียวกัน ในการทดลองของเขา เขาได้ใช้เครื่องมือเป็นหลอดแก้วรูปตัวเจ(J form) คล้ายๆ กับของ โรเบิร์ต บอยล์ ภายในหลอดบรรจุแก๊สปริมาณหนึ่งเอาไว้ เมื่อเขาให้ความร้อนแก่แก๊สที่อยู่ในหลอด เขาพบว่าแก๊สได้ขยายตัวมีปริมาตรเพิ่มขึ้น
จากการทดลองของชาร์ล พบว่าปริมาตรของแก๊สจะเพิ่มขึ้น ตามอุณหภูมิที่เพิ่มขึ้น และในทางตรงกันข้ามถ้าลดอุณหภูมิลงปริมาตรของแก๊สก็จะลดลงด้วย มีลักษณะเช่นเดียวกับรูปด้านบน
โดยเขาพบว่า ถ้าตอนเริ่มต้นทดลอง อุณหภูมิของแก๊ส อยู่ที่ 0 องศาเซลเซียส และปริมาตรแก๊สเริ่มต้นที่ค่าหนึ่ง
- ถ้าให้อุณหภูมิเพิ่มขึ้นไปเป็น 1 องศาเซลเซียส ปริมาตรของแก๊สจะเพิ่มขึ้นจากเดิมประมาณ![]() เท่า
เท่า
- ถ้าอุณหภูมิเพิ่มขึ้นไปเป็น 2 องศาเซลเซียส ปริมาตรแก๊สจะเพิ่มจากเดิมประมาณ ![]() เท่าและ
เท่าและ
- ถ้าอุณหภูมิเพิ่มไปเป็น 10 องศาเซลเซียส ปริมาตรแก๊สเพิ่มจากเดิมอีกประมาณ ![]()
สัดส่วนนี้จะเป็นไปตามอุณหภูมิที่เพิ่มขึ้นนั้น ปริมาตรจะแปรผันตรงตามอุณหภูมิ เรากำหนดให้ค่าสัดส่วน ![]() เป็นค่าคงที่ค่าหนึ่งใช้สัญลักษณ์เป็น แอลฟา(
เป็นค่าคงที่ค่าหนึ่งใช้สัญลักษณ์เป็น แอลฟา(![]() ) โดยค่า
) โดยค่า ![]() ซึ่งเศษส่วนนี้ในความรู้สึกของเราก็ถือว่าน้อยมาก แต่ถ้าอุณหภูมิเปลี่ยนมากๆ ค่าเศษส่วนนี้ก็จะมีค่ามากขึ้น เช่น จาก 0 องศาเซลเซียส เพิ่มอุณหภูมิให้แก๊สขึ้นไปเป็น 100 องศา ปริมาตรแก๊สก็จะเปลี่ยนไปจากเดิมประมาณ
ซึ่งเศษส่วนนี้ในความรู้สึกของเราก็ถือว่าน้อยมาก แต่ถ้าอุณหภูมิเปลี่ยนมากๆ ค่าเศษส่วนนี้ก็จะมีค่ามากขึ้น เช่น จาก 0 องศาเซลเซียส เพิ่มอุณหภูมิให้แก๊สขึ้นไปเป็น 100 องศา ปริมาตรแก๊สก็จะเปลี่ยนไปจากเดิมประมาณ ![]() ของหน่วยปริมาตร หรืออีกกรณีหนึ่ง ถ้าแก๊สมีปริมาณเยอะมาก ปริมาตรเริ่มต้นของแก๊สมีขนาดใหญ่ ก็จะทำให้เกิดการเปลี่ยนแปลงที่เราสังเกตได้ชัดเจนขึ้น กำหนดให้สัดส่วนเป็นค่าแอลฟา (
ของหน่วยปริมาตร หรืออีกกรณีหนึ่ง ถ้าแก๊สมีปริมาณเยอะมาก ปริมาตรเริ่มต้นของแก๊สมีขนาดใหญ่ ก็จะทำให้เกิดการเปลี่ยนแปลงที่เราสังเกตได้ชัดเจนขึ้น กำหนดให้สัดส่วนเป็นค่าแอลฟา (![]() ) และเมื่อนำข้อมูลการทดลองของชาร์ลไปเขียนกราฟความสัมพันธ์ระหว่างปริมาตรและอุณหภูมิในหน่วยองศาเซลเซียสจะได้กราฟดังรูป
) และเมื่อนำข้อมูลการทดลองของชาร์ลไปเขียนกราฟความสัมพันธ์ระหว่างปริมาตรและอุณหภูมิในหน่วยองศาเซลเซียสจะได้กราฟดังรูป
เราจะได้กราฟเส้นตรง จุดตัดแกน y คือปริมาตรของแก๊สที่ อุณหภูมิ 0 องศาเซลเซียส ให้เท่ากับ V0 มิลลิลิตรและเมื่อลากเส้นประไปจนปริมาตรของแก๊สเท่ากับ 0 มิลลิลิตรพบว่าเส้นกราฟตัดแกนอุณหภูมิที่ประมาณ -273 องศาเซลเซียส
จากกราฟเส้นตรงที่ได้จากการทดลองเขียนเป็นความสัมพันธ์ทางคณิตศาสตร์ระหว่างปริมาตรและอุณหภูมิได้ดังนี้
![]()
เมื่อ V = ปริมาตรของแก๊สที่สังเกต ณ อุณหภูมิใดๆ
V0 = ปริมาตรแก๊สที่ 0 องศาเซลเซียส
t = อุณหภูมิในหน่วยองศาเซลเซียส
คูณ ![]() เข้าไปจะได้
เข้าไปจะได้
![]() ....................................................1
....................................................1
เมื่อแทนค่า ![]() ในสมการ 1 จะได้
ในสมการ 1 จะได้
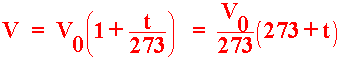 ........................................(2)
........................................(2)
และกำหนดให้ ![]() สมการ (2) จะกลายเป็น
สมการ (2) จะกลายเป็น
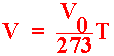 ....................................................................(3)
....................................................................(3)
หรือ ![]() ...................................................(4)
...................................................(4)
เมื่อ k เป็นค่าคงที่
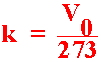
และ T ก็จะเป็นอุณหภูมิทำให้ปริมาตรของแก๊สแปรผันตรงแบบเป็นเส้นตรง
จากสมการ (3) จะพบว่าถ้า แก๊สมีปริมาตร(V) เท่ากับ 0 พจน์ T จะต้องเป็น 0 ด้วย (เพราะ k เป็นค่าคงที่มากกว่า 1 ) นั่นแสดงว่าอุณหภูมิในหน่วยองศาเซลเซียสที่ทำให้แก๊สมีปริมาตรเป็น 0 จริงๆ จะเท่ากับ
T = 273 + t
เมื่อ T = 0 ; 0 = 273+t
นั่นหมายความว่า t = -273 องศาเซลเซียส
ที่อุณหภูมิ -273 องศาเซลเซียสแก๊สจะมีปริมาตรเป็น 0 ซึ่งอุณหภูมินี้เป็นอุณหภูมิ 0 ที่แท้จริง ดังนั้นจึงกำหนดให้ที่อุณหภูมินี้เป็นหน่วยอุณหภูมิที่เริ่มจาก 0 จริงๆ และหน่วยอุณหภูมิใหม่ นี้คือ เคลวิน (K)นั่นเอง
กลับไปที่เนื้อหา
บทเรียนที่ 3 กฏของอาโวกาโดร
|
อาเมเดโอ อาโวกาโดร นักวิทยาศาสตร์ชาวอิตาลีชื่อ อาเมเดโอ อาโวกาโดร ได้ศึกษาความสัมพันธ์ระหว่างปริมาตรกับปริมาณของแก๊ส โดยเขาได้เสนอสมมติฐานไว้ในปี ค.ศ. 1811 ว่า "ที่อุณหภูมิและความดันเดียวกัน แก๊สต่างชนิดกันที่มีปริมาตรเท่ากันจะมีจำนวนโมเลกุลเท่ากัน" ซึ่งหมายความว่า แก๊สทุกชนิดจะมีปริมาตรเพิ่มขึ้นเรื่อยๆ เมื่อจำนวนโมเลกุลของแก๊สเพิ่มขึ้นเรื่อยๆ เช่นกัน แต่ข้อสมมติฐานของเขาไม่ได้รับการยอมรับจากวงการวิทยาศาสตร์ในสมัยนั้นเป็นเวลาเกือบ 50 ปี และต่อมาเมื่อ สตานิซาโล คานนิซาโร(Stanisalo Cannizaro) ได้ทดลองพิสูจน์และได้นำเสนอในที่ประชุมวิทยาศาสตร์เมื่อปี ค.ศ. 1860 สมมติฐานของอาโวกาโดรจึงได้รับการยอมรับในที่สุด และเพื่อเป็นเกียรติแก่อาโวการโดร ตัวเลข 1 โมลซึ่งเท่ากับ 6.02 x 1023 จึงเรียกว่า เลขอาโวกาโดร (Avogadro Number) จากข้อสมมติฐานของอาโวกาโดรเมื่อได้ทดลองซ้ำต่อมาหลายๆ ครั้งก็ยืนยันความสัมพันธ์ที่เป็นไปตามสมมติฐานอาโวกาโดร จึงตั้งเป็นกฏของอาโวกาโดรขึ้นมา ซึ่งกล่าวว่า "ที่ความดันและอุณหภูมิของแก๊สคงที่ ปริมาตรของแก๊สจะแปรผันตรงกับจำนวนโมเลกุลหรือจำนวนโมลของแก๊สนั้น" ดังแผนภาพด้านล่าง
เมื่อ n คือจำนวนโมล และ V คือปริมาตรของแก๊ส จากแผนภาพ เมื่อ n มีจำนวนน้อย V ก็จะน้อยด้วย แต่เมื่อ n มีจำนวนมากขึ้น V ก็จะมากขึ้นตามไปด้วย จากสมมติฐานของอาโวกาโดรเขียนเป็นความสัมพันธ์ทางคณิตศาสตร์ได้ว่า ปริมาตรของแก๊ส แปรผันตรงกับจำนวนโมลของแก๊ส
|
กลับไปที่เนื้อหา
บทเรียนที่ 4 กฎของแก๊สอุดมคติ
|
จากการทดลองและข้อสรุปของนักวิทยาศาสตร์หลายๆ คนที่ศึกษาเรื่องแก๊สเราจะเห็นว่า สมบัติของแก๊สมีความสัมพันธ์กันด้วยตัวแปรคล้ายๆ กัน คือ ทุกคนต่างก็ดูที่ปริมาตรของแก๊สที่เปลี่ยนไป ด้วยการกำหนดตัวแปรต้นแตกต่างกันออกไป บอยล์ เมื่อเปลี่ยนความดันของแก๊ส ปริมาตรจะเป็นอย่างไร ชาร์ล เมื่อเปลี่ยนอุณหภูมิของแก๊ส ปริมาตรจะเป็นอย่างไร อาโวกาโดร เมื่อเปลี่ยนจำนวนโมลหรือจำนวนโมเลกุลของแก๊ส ปริมาตรจะเป็นอย่างไร และทุกคนก็ได้ข้อสรุปดังที่ได้นำเสนอกฏของทุกคนมาแล้ว ถ้าเรารวบรวมกฎที่เกี่ยวกับแก๊สที่กล่าวมาแล้วทั้งหมด เราจะได้ความสัมพันธ์ดังนี้ จาก กฏของบอยล์ กฎของชาร์ล กฏของอาโวกาโดร เราสามารถรวมกฎทั้งสามนี้เข้าเป็นสมการรวมเพียงสมการเดียวได้ดังนี้
เมื่อ
สมการนี้เรียกว่า สมการแก๊สในอุดมคติ R = ค่าคงที่ของแก๊ส (gas constant) จากตัวแปรทั้ง 4 ตัว คือ ความดัน(P), ปริมาตร(V), จำนวนโมล(n) และอุณหภูมิ(T) เราสามารถหาค่า R ได้จากการแทนค่าตัวแปรทั้งสี่ในสมการแก๊สอุดมคติ แก๊สอุดมคติ 1 โมล ที่สภาวะมาตรฐาน ความดันเท่ากับ 1 บรรยากาศ อุณหภูมิ 273 K มีปริมาตร 22.4 ลิตร เราจะสามารถคำนวณหาค่าคงที่ของแก๊สได้ดังนี้ จาก
นอกจากนี้ค่าคงที่ R ยังมีได้อีกในหลายหน่วย ดังนี้
แก๊สใดๆ ก็ตามที่มีพฤติกรรมเป็นไปตามกฏนี้ จะเรียกแก๊สนั้นว่าแก๊สที่มีพฤติกรรมในอุดมคติ หรือแก๊สอุดมคติ หรือแก๊สสมบูรณ์แบบ (ideal gas) ตัวอย่างการใช้กฎของแก๊สอุดมคติ ในการคำนวณ ตัวอย่าง 1 น้ำจำนวน 1 กรัม ระเหยกลายเป็นไอในภาชนะขนาด 10 ลิตร ความดันของน้ำจะเป็นเท่าใดเมื่อการระเหยเป็นไอสมบูรณ์ที่อุณหภูมิ 200 องศาเซลเซียส วิธีคำนวณ จาก เราต้องการหาความดันของไอน้ำ จำนวนโมล (n) ของน้ำ
และอุณหภูมิสัมบูรณ์ เท่ากับ
แทนค่า V = 10 L , T = 473 K และ n = 0.056 mol ความดันจะเท่ากับ
ตัวอย่าง 2 บอลลูนลูกหนึ่งบรรจุแก๊สฮีเลียม (He) หนัก 30 กิโลกรัม บอลลูนลูกนี้จะมีปริมาตรเท่าใด ถ้าความดันของแก๊สฮีเลียมเป็น 1.15 atm ณ อุณหภูมิ 20 องศาเซลเซียส วิธีทำ จาก เราอยากทราบปริมาตรของบอลลูน ก่อนอื่นต้องคำนวณหา จำนวนโมลของแก๊สฮีเลียม หนัก 30 กิโลกรัม ก่อน เราทราบมาแล้วว่า ฮีเลียมจำนวน 1 โมล มีน้ำหนัก 4 กรัม หรือ 0.0040 kg
อุณหภูมิต้องเปลี่ยนเป็นหน่วยเคลวินก่อน
ดังนั้น ปริมาตรสามารถคำนวณได้ดังนี้
|
กลับไปที่เนื้อหา
บทเรียนที่ 5 กฎการแพร่ของเกรแฮม
![]()
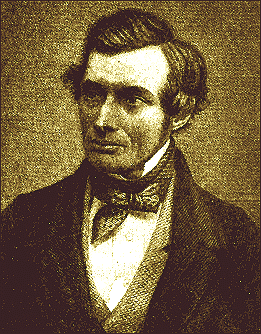
โทมัส แกรห์ม (Thomas Graham) ค.ศ.1805 -1869)
การแพร่ (diffusion) ของสารต่างๆ หมายถึง อนุภาคของสารนั้นเคลื่อนที่ไปจากบริเวณที่มีความเข้มข้นสูงไปยังบริเวณความเข้มข้นต่ำกว่า ในกรณีของแก๊ส ก็หมายถึง การที่โมเลกุลของแก๊สชนิดหนึ่งเคลื่อนที่กระจายออกไปจากบริเวณที่มีความหนาแน่นมากไปหาบริเวณที่มีความหนาแน่นน้อยกว่าและหลังจากนั้นแก๊สก็จะกระจายตัวให้มีความเข้มข้นโดยเฉลี่ยทุกบริเวณเท่าๆกัน การแพร่ก็จะสามารถเกิดขึ้นได้ต่อเนื่องจนระดับความเข้มข้นของแก๊สทุกบริเวณที่แก๊สไหลไปได้นั้นมีค่าเท่ากัน แก๊สจึงจะหยุดแพร่ แต่แก๊สก็มีการเคลื่อนที่ตลอดเวลา โดยแก๊สที่ผสมกันต้องไม่เกิดปฏิกิริยาเคมีกัน ดังนั้น การแพร่ของแก๊สนี้จึงเป็นการเปลี่ยนแปลงทางกายภาพอย่างเดียว ไม่มีปฏิกิริยาเคมีเกิดขึ้น
ถึงแม้ว่าโมเลกุลของแก๊สจะเคลื่อนที่ด้วยความเร็วสูงมาก แต่ก็เป็นการเคลื่อนที่แบบสุ่ม ดังรูปข้างล่าง กว่าจะถึงจุดหมายปลายทาง ถ้าดูแต่ละอะตอม หรือโมเลกุลของแก๊ส จะพบว่าระหว่างทางต้องเจออุปสรรคมากมายจากการชนกับโมเลกุลแก๊สชนิดเดียวกันหรือแก๊สชนิดอื่น รวมทั้งเกิดการชนผนังภาชนะอีกด้วย ทำให้กว่าจะไปถึงที่หมายต้องเสียเวลาไปชนตัวนั้น เฉียดตัวนี้
คำว่าอัตราการแพร่ (r) ก็คือดูแก๊สเดินทางจาก จุด A ไป B ด้วยอัตราเร็วเท่าไหร่ในหนึ่งหน่วยเวลา เช่นเดียวกับการถามว่า รถเมล์สายนี้วิ่งเร็วเท่าไหร่ แต่ในกรณีของแก๊สระหว่างทางจะเกิดการชนกับโมเลกุลอื่นๆไปด้วย พร้อมกับเคลื่อนที่ไปพร้อมกับการชนกับโมเลกุลอื่นพร้อมๆ กันลักษณะนี้จึงเรียกว่าการแพร่ (diffusion)
การไหลเข้ามาผสมกันของแก๊สสองชนิดมีพฤติกรรมเป็นอย่างไร มีปัจจัยใดบ้างที่ต้องพิจารณากัน
เราอยากทราบพฤติกรรมการแพร่ของแก๊สชนิดต่างๆ ว่าจะเหมือนหรือแตกต่างกันอย่างไร มาพิจารณารูปด้านล่าง
รูปด้านล่างแสดงการแพร่เข้าหากันของแก๊สสองชนิด แก๊สชนิดสีแดงกับแก๊สสีน้ำเงิน สมมติให้แก๊สสีแดงมีมวลมากกว่าแก๊สสีน้ำเงิน แก๊สสองชนิดนี้มีอัตราการแพร่ที่แตกต่างกัน อัตราการไหลของแก๊สทั้งสองชนิดที่แตกต่างกันนี้เป็นเพราะอะไร
เมื่อปี ค.ศ. 1832 นักเคมีชาวสก๊อต ชื่อว่า ทอมัส แกรห์ม ได้ทำการศึกษาแก๊ส และพบว่า ภายใต้สภาวะอุณหภูมิและความดันเดียวกัน อัตราการแพร่ของแก๊สจะเป็นสัดส่วนผกผันกับรากที่สองของมวลแก๊สนั้นต่อโมล
นั่นหมายความว่า แก๊สที่มีน้ำหนักมากกว่าจะเคลื่อนไหวได้ช้ากว่าแก๊สที่เบากว่า เหมือนแก๊สสีแดงจากรูปด้านบนมีขนาดใหญ่มีน้ำหนักมากจะเคลื่อนที่ผ่านรูได้ช้ากว่าแก๊สสีน้ำเงินซึ่งมีน้ำหนักน้อยกว่า
เนื่องจากมวลมีความสัมพันธ์กับความหนาแน่นโดยตรง ถ้ากำหนดให้แก๊สสองชนิดมีปริมาตรเท่ากัน จะพบว่าแก๊สที่มีมวลมากกว่าจะมีความหนาแน่นมากกว่าแก๊สที่มีมวลน้อย ดังนั้นเราจึงแสดงได้ในเทอมของความหนาแน่นได้ อัตราการแพร่ของแก๊สเป็นสัดส่วนผกผันกับรากที่สองของความหนาแน่นของแก๊สนั้นเช่นเดียวกับมวลหรือมวลโมเลกุล
|
อัตราการแพร่ =
|
เมื่อ
|
กำหนดให้
|
r1= อัตราเร็วของแก๊สชนิดที่หนึ่ง r2 = อัตราเร็วของแก๊สชนิดที่สอง d1 = ความหนาแน่นของแก๊สชนิดที่หนึ่ง d2 = ความหนาแน่นของแก๊สชนิดที่สอง k = ค่าคงที่ของการแพร่ |
จะได้ว่า
|
จะได้ว่า
จะได้
เอาสมการ (1) หาร (2)
เนื่องจากความหนาแน่นเป็นสัดส่วนโดยตรงกับมวลโมเลกุลที่ P และ T คงที่ จาก
จะเห็นได้ว่า ความหนาแน่น ( ดังนั้น จาก
|
พฤติกรรมของแก๊สลักษณะนี้ สามารถนำไปใช้หาอัตราการแพร่ของแก๊ส 2 ชนิดที่มีมวลแตกต่างกันได้ แม้แต่มวลที่ต่างกันน้อยมาก เช่น นำไปใช้แยกไอโซโทปของยูเรเนียมในสารประกอบยูเรเนียมเฮกซะฟลูออไรด์ (UF6) ของ U-235 ออกจาก U-238 โดยการใช้หลักการแพร่นี้
การแพร่ผ่าน (effusion) คือปรากฏการณ์ที่แก๊สเคลื่อนที่จากบริเวณหนึ่งที่มีความเข้มข้นของแก๊สสูงกว่า ผ่านรูเล็กๆ ไปยังบริเวณที่มีแก๊ส มีความเข้มข้นน้อยกว่าหรือยังไม่มีแก๊สชนิดนั้นอยู่
การแพร่ในลักษณะนี้จึงเรียกว่าการแพร่ผ่าน ซึ่งก็คือปรากฏการณ์ที่แก๊สเคลื่อนจากบริเวณหนึ่งผ่านรูเล็กๆ ไปยังบริเวณแก๊สที่มีความเข้มข้นน้อยกว่าหรือบริเวณที่ไม่มีแก๊สชนิดนั้นอยู่ โดยขณะที่แก๊สแพร่ผ่านไปจะเกิดการชนกันระหว่างโมเลกุลหรือชนผนังภาชนะไปด้วย
ส่วนรูปด้านบนนี้เป็น การสาธิต การแพร่ผ่าน จากรูปโมเลกุลแก๊สสีแดงแพร่จากกล่องด้านซ้ายมือแพร่ผ่านรูเล็กๆ ไปยังบริเวณกล่องที่เป็นสูญญากาศด้านขวามือ
กลับไปที่เนื้อหา
บทเรียนที่ 6 ทฤษฏำจลน์โมเลกุลของแก๊ส
![]()
หลายคนอาจจะสงสัยมาโดยตลอดว่า ทำไมแก๊สถึงมีปริมาตร ทำไมแก๊สถึงอยู่ในภาชนะได้ทั่วทั้งภาชนะ ทำไมอนุภาคแก๊สไม่ตกลงไปรวมกันอยู่ที่ก้นของภาชนะ ในเมื่อแก๊สก็มีมวลเช่นเดียวกับของแข็ง ของเหลว ก็น่าจะถูกแรงโน้มถ่วงของโลกดึงลงเหมือนกัน
การตอบคำถามเหล่านี้ จึงทำให้มีการทดลองและศึกษาและรวบรวมข้อมูลมาเขียนเป็นเรื่องราวเพื่อใช้อธิบายพฤติกรรมเหล่านี้ ในศตวรรษที่ 19 นักฟิสิกส์หลายคน โดยเฉพาะอย่างยิ่ง ลุดวิก เอดูอาล โบลต์ซมานน์ (Ludwig Eduard Boltzmann) และ เจมส์ คลาร์ก แมกซ์เวลล์ (James Clerk Maxwell) พบว่าสมบัติทางกายภาพของแก๊สนั้นอธิบายได้จากการเคลื่อนที่ของแต่ละโมเลกุลของแก๊สเหล่านั้น
ในที่สุด ผลงานของแมกซ์เวลล์และโบลต์ซมานน์ และนักวิทยาศาสตร์อีกหลายคน ก็ได้กลายเป็นทฤษฎีสำคัญที่ใช้อธิบายพฤติกรรมของแก๊ส เรียกว่า ทฤษฎีจลน์โมเลกุลของแก๊ส หรือเรียกว่า ทฤษฎีจลน์ของแก๊ส
ทฤษฎีจลน์ของแก๊สเป็นทฤษฎีเพื่อใช้อธิบายพฤติกรรมของแก๊สโดยการใช้แบบจำลองหรือทฤษฎีในระดับจุลภาค (microscopic model) คือพิจารณาคุณสมบัติของโมเลกุลของแก๊สเพียงหนึ่งหรือสองโมเลกุลเพื่อเป็นตัวแทนของโมเลกุลล้านๆโมเลกุลในระดับมหภาค (macroscopic model) (สมบัติมหภาคคือสมบัติที่แก๊สแสดงให้เราเห็นว่าแก๊สมีปริมาตร มีความดัน มีความหนืด มีการไหล การนำพาความร้อน เป็นต้น ซึ่งเป็นสมบัติที่โมเลกุลของแก๊สเป็นล้านๆ โมเลกุลรวมกันเหล่านั้นแสดงออกมา) เมื่อเราพิจารณาโมเลกุลแก๊สจำนวนน้อยๆ เป็นตัวแทนของกลุ่มประชากรทั้งหมด จึงหลีกเลี่ยงไม่ได้ที่จะต้องมีศาสตร์ทางคณิตศาสตร์และสถิติเข้ามาเกี่ยวข้อง เช่น จำเป็นต้องมีค่าเฉลี่ย มีความน่าจะเป็น เป็นต้น เพราะว่าข้อมูลที่ได้มานั้นเป็นข้อมูลของกลุ่มตัวอย่างแก๊ส ไม่ใช่ประชากรทั้งหมด
ทฤษฎีจลน์โมเลกุลของแก๊ส มีพื้นฐานสำคัญอยู่ที่หลักที่ว่าอนุภาคของแก๊สมีการเคลื่อนที่อยู่ตลอดเวลา เมื่อแก๊สมีการเคลื่อนที่ก็ย่อมมีพลังงานอยู่ในโมเลกุล การเคลื่อนที่ของโมเลกุลแก๊สดังกล่าวนี้เป็นพลังงานรูปหนึ่งซึ่งเราอาจให้นิยามว่าเป็นความสามารถในการทำงานหรือในการทำให้เกิดการเปลี่ยนแปลง พลังงานมีหลายชนิด พลังงานที่เกี่ยวข้องกับการเคลื่อนที่ของวัตถุต่างๆ เรียกว่า พลังงานจลน์ (kinetic energy)หรืออาจกล่าวได้ว่า พลังงานจลน์ คือพลังงานของการเคลื่อนที่ ดังนั้น เมื่อแก๊สมีการเคลื่อนที่ตลอดเวลาก็ ย่อมมีพลังงานจลน์อยู่ในตัวด้วย
ทฤษฎีจลน์โมเลกุลของแก๊สมีเนื้อหาสรุปบนสมมติฐานต่างๆ ได้ดังนี้
1. แก๊สประกอบด้วยอนุภาคที่เล็กมาก อนุภาคคือโมเลกุล แต่ละโมเลกุลของแก๊สอยู่ไกลกันมากเมื่อเทียบกับขนาดของโมเลกุล จนถือว่าโมเลกุลเป็นจุดทรงกลมแข็งเล็กๆ
2. โมเลกุลของแก๊สมีการเคลื่อนที่ตลอดเวลา การเคลื่อนที่ของโมเลกุลเป็นแบบสุ่ม และเกิดการชนกันระหว่างโมเลกุลแก๊สบ่อยครั้งมาก
3. ไม่มีแรงกระทำระหว่างโมเลกุล ยกเว้นเมื่อเกิดการกระทบกัน และเมื่อโมเลกุลเข้าชนกัน จะชนแบบยืดหยุ่น(elastic collision)
การชนแบบยืดหยุ่นคือ ผลรวมของพลังงานจลน์ก่อนการชนจะมีค่าเท่ากับผลรวมของพลังงานจลน์หลังการชน นั่นคือมีการอนุรักษ์พลังงานจลน์ไว้ ตัวอย่างการชนแบบยืดหยุ่นแสดงในรูปด้านล่าง
แม้จะมีการถ่ายเทพลังงานให้กันแต่สุดท้ายเมื่อคิดพลังงานจลน์รวมของโมเลกุลทั้งสองแล้วพลังงานจลน์รวมก่อนการชนและหลังการชนจะไม่เปลี่ยนแปลงหมายความว่า ถ้าโมเลกุลหนึ่งให้พลังงาน อีกโมเลกุลหนึ่งก็ต้องรับพลังงานด้วยปริมาณที่ให้และรับเท่าๆ กัน หรือถ้ามีหลายๆ โมเลกุล เมื่อโมเลกุลเกิดการชนกัน พลังงานจะถ่ายเทไปมาระหว่างโมเลกุล ผลรวมของพลังงานจลน์ทั้งหมดจะเท่าเดิมตลอดเมื่อเวลาผ่านไป
4. พลังงานอย่างเดียวที่แก๊สมีคือพลังงานของการเคลื่อนที่ไปมาของแก๊สนั่นคือพลังงานจลน์
ในความเป็นจริงแล้วแบบจำลองที่กล่าวมาทั้ง 4 ข้อดังกล่าวไม่ถูกต้องนัก เพราะ
โมเลกุลไม่เป็นรูปร่างทรงกลมแข็ง โมเลกุลยังมีพลังงานนอกเหนือจากพลังงานจลน์อีก นั่นคือโมเลกุลแก๊สมีพลังงานภายในอยู่ด้วย ซึ่งต้องใช้วิชากลศาสตร์ควอนตัม(quantum mechanics) ในการคำนวณหาค่าพลังงานเหล่านั้น โมเลกุลยังมีแรงดึงดูดและแรงผลักกันอยู่ การเข้าชนกันของโมเลกุลจึงไม่ได้เป็นแค่การสัมผัสเฉยๆ แต่หมายถึงการเข้ามาชนกันด้วยระยะที่แตกต่างกันออกไปทำให้อาจเกิดแรงดึงดูดหรือแรงผลักมากขึ้นหรือลดลง นอกจากนั้นการชนกันของโมเลกุลแก๊สยังไม่ใช่การชนแบบยืดหยุ่นด้วย แล้วคำอธิบายที่ถูกต้องกว่าอยู่ที่ไหนหล่ะ.............
ตามไปดูที่พฤติกรรมของแก๊สจริง ต่อไปครับ
กลับไปที่เนื้อหา
-
7199 กฏของแก๊สจริงและแก๊สอุดมคติ /lesson-chemistry/item/7199-2017-06-09-12-53-25เพิ่มในรายการโปรด